Воднева корозія воднева корозія - пошкодження стали і її охрупчивание під
Воднева корозія - пошкодження стали і її охрупчивание під впливом тривалого впливу водневої середовища при підвищених (gt; 200 ° С) температурах експлуатації в результаті фізико-хімічної взаємодії водню з окремими компонентами та / або фазами сплаву. Водневе пошкодження при підвищених температурах пов'язано з утворенням продуктів реакції між воднем і вуглецем за типом
В вуглецевої сталі сумарна хімічна реакція між вуглецем, пов'язаним в карбідах заліза, і воднем може бути представлена у вигляді

Утворений в результаті реакції метан залишає метал і / або утворює внутрішні порожнини і тріщини, наповнені газоподібним метаном під високим тиском. У поверхневих шарах металу формуються зневуглецьована зони, типу представленої на рис. 4.40, б. Воднева корозія може протікати у всіх сталях, якщо вони містять вуглець в доступній для реакції формі і він досить рухливий, щоб вступати в реакцію з воднем.
Сприйнятливість стали до водневої корозії залежить від легуючих елементів, які впливають на активність вуглецю. Швидкість водневої корозії залежить від тиску водню і температури, а також від розміру зерен, складу їх кордонів, ступеня наклепу стали і інших чинників.
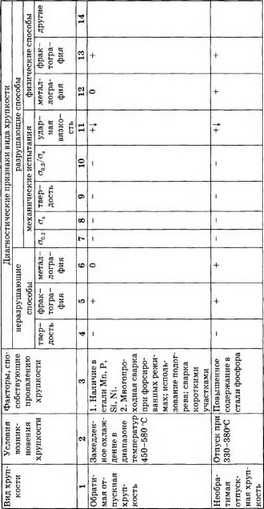
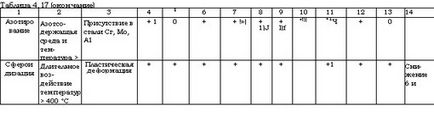
де k - коефіцієнт пропорційності.
Для запобігання водневої корозії використовують легування стали. Введення карбидообразующих елементів, таких як Сг, Мо, W, Та й V, істотно підвищує стійкість стали проти цього виду ушкодження і охрупчивания [82]. Вплив зазначених вище елементів пов'язано з освітою в стали при її легуванні стійких карбідів.
Воднева корозія необоротна і ніякої термічною обробкою не вдається відновити початкові властивості металу. На відміну від водневої крихкості класичного типу, коли НЕ
Відповідно до сучасних уявлень, накопичення метану в окремих зонах металу здатне досягати сотень мегапаскалей, обумовлюючи виникнення напружень, що перевищують тимчасовий опір стали.
За даними [121], в стали 45 при 600 ° С в середовищі водню при тиску 49 МПа рівноважний тиск метану в мікропорах досягає 117,6 ГПа. У високолегованої сталі 4Х25Н20С2 це тиск одно лише 1,88 МПа. Період, протягом якого відбуваються локалізовані хімічні реакції і накопичення продуктів цих реакцій, але не спостерігається помітного зниження міцності і пластичних властивостей стали, називають інкубаційним [120].
За розрахунками [121], для вуглецевої (0,39% С) і низьколегованої (0,34% С, 0,5% Мо) сталей в середовищі водню при 9,8 МПа і 500 ° С для створення критичного тиску метану 98 МПа в сферичних мікропорах радіусом 50 мкм необхідно 0,1 нг вуглецю. При товщині навколишнього мікропорами обезуглероженного шару -0,1 мм час дифузії вуглецю 2 ч. Це на два порядки менше тривалості інкубаційного періоду, отриманої в експерименті.
На другому етапі впливу водню на сталь тиск продуктів реакції (головним чином, метану) викликає зниження когезивних міцності кордонів зерен. Розвиток цього процесу призводить до виникнення мікроскопічних тріщин і виходу продуктів реакції по тріщинах з металу. Водень, хемосорбірованний на поверхнях окремих мікропорожнин, також ініціює процес розтріскування, внаслідок зменшення поверхневої енергії тріщин.