Умови освіти аморфної структури
Що собою являє вода? Абсолютно хаотичне скупчення молекул Н2 О. Але якщо охолодити воду до 0 ° С, то її замерзають молекули проявлять прагнення зайняти вже не будь-яке випадкове положення, а лише те, що відповідає кристалічній решітці льоду. Так непримітна крапелька дощу перетворюється на красеня-сніжинку. В результаті цієї перебудови суттєво змінюються не тільки стан, а й багато фізико-хімічні властивості речовини.
З іншого боку, серед твердих тіл зустрічаються і такі, які «не визнають» кристалічну структуру. Так, скло аморфно і в рідкому, і в твердому стані, тому аморфний стан часто називають стеклообразном. А чи не можна аморфний металевий розплав змусити перейти в тверде, але теж аморфний стан, тобто отримати металеве «скло»?
При звичайній кристалізації, яка протікає в часі, атоми речовини мають можливість «подумати» над тим, як їм поводитися під час перебудови. Завдяки цьому вони встигають зайняти в просторі належні їм місця. Якщо ж речовина змусити миттєво затвердіти, то атоми будуть змушені залишатися на місці.
В отриманні металевих гранул застосовуються швидкості охолодження металу в десятки і сотні тисяч градусів в секунду. Воістину фантастичні швидкості, але навіть вони могли забезпечити металу лише микрокристаллическую структуру, але не аморфну. Отже, потрібна ще б # 972; більша швидкість відводу тепла від металевого розплаву - мільйон градусів в секунду. Чи реально це?
Така швидкість цілком досяжна, якщо, наприклад, закликати на допомогу глибокий вакуум і криогенні температури. При нанесенні паровметалла на переохолоджену металеву пластинку, що знаходиться в камері, де створені зазначені умови, на ній утворюється найтонший «скляний» шар. Уже перші дослідження дали дуже обнадійливі результати: наприклад, плівка «скляного» вісмуту, втративши своєї кристалічної структури, знайшла натомість цінні електричні і магнітні властивості, що не спостерігаються у того ж металу в звичайному стані. Так, навіть при кімнатній температурі електроопір аморфної плівки товщиною всього в декілька мікрон у багато разів нижче, ніж у кристалічного вісмуту.
Використання спеціальних методів дозволяє досягати швидкості охолодження більше 10 5 Я на / с і отримувати метал в склоподібного аморфному стані.
На рис. 13 представлено схематичне зображення ТТТ діаграми (temperature-time-transformation), яка показує характер фаз, що утворюються в сплаві при різних швидкостях охолодження. При переохолодженні рідкої фази нижче рівноважної температури плавлення ТПЛ швидкість кристалізації досягає максимуму при температурі ТП. Якщо рідина загартувати зі швидкістю вище критичної до температури склування ТД. то система буде «заморожена» і утворюється аморфний стан. Критична швидкість охолодження для різних аморфних сплавів становить від 10 2 до 10 10 К / с.
З діаграми також випливає, що якщо аморфний сплав згодом нагріти до температури Т <ТП и выдерживать изотермически в течение времени t К ; он начнет кристаллизоваться. Если же аморфный сплав медленно нагревать от комнатной температуры, то кристаллизация начинается при температуре ТХ. которая повышается по мере увеличения скорости нагрева. Условия перехода в кристаллическое состояние меняются в широких пределах для разных аморфных систем.
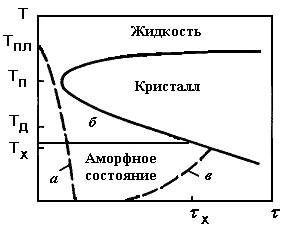
а - критична швидкість охолодження з отриманням аморфного стану; б - ізотермічний отжиг аморфного стану, що приводить до кристалізації в період часу t К; в - повільний нагрів аморфного стану, що веде до кристалізації при температурі Тх
Мал. 13. Схема діаграми процесу освіти фаз в переохолодженому розплаві
Структура аморфних сплавів подібна до структури замороженої рідини. Затвердіння відбувається настільки швидко, що атоми речовини виявляються замороженими в тих положеннях, які вони займали, будучи в рідкому стані. Аморфна структура характеризується відсутністю далекого порядку в розташуванні атомів, завдяки чому в ній немає кристалічної анізотропії, відсутні границі блоків зерен і інші дефекти структури, типові для полікристалічних сплавів.
Наслідком такої аморфної структури є незвичайні магнітні, механічні, електричні властивості і корозійна стійкість аморфних металевих сплавів. Поряд з високою магнітною м'якістю (рівень електромагнітних втрат в аморфних сплавах з високою магнітною індукцією істотно нижче, ніж у всіх відомих кристалічних сплавах), ці матеріали виявляють виключно високу твердість і міцність при розтягуванні, в ряді випадків мають близький до нуля коефіцієнт теплового розширення, а питомий електроопір в 3-4 рази вище, для заліза і його сплавів. Деякі з аморфних сплавів характеризуються високу корозійну стійкість.
Затвердіння з утворенням аморфної структури принципово можливо для всіх металів і сплавів. Для практичного застосування у звичайних випадках використовують сплави перехідних металів (Fe, Co, Mn, Cr, Ni та ін), в які для освіти аморфної структури добавляютаморфообразующіе елементи (В, С, Si, P, S). Такі аморфні сплави зазвичай містять близько 80% (ат.) Одного або декількох перехідних металів і 20% неметалів, що додаються для освіти і стабілізації аморфної структури. Склад аморфних сплавів близький до формулеM80 Х20. де М - один або кілька перехідних металів, а Х - один або кілька аморфізаторов. Відомі аморфні сплави, склад яких відповідає наведеній формулі: Fe70 Cr10 P15 B5. Fe40 Ni40 S14 В6. Fe80 P13 B7 і ін. Аморфізатори знижують температуру плавлення і забезпечують досить швидке охолодження розплаву нижче його температури склування так, щоб в результаті утворилася аморфна фаза. На термічну стабільність аморфних сплавів має найбільший вплив кремній і бор, найбільшою міцністю володіють сплави з бором і вуглецем, а корозійна стійкість залежить від концентрації хрому і фосфору.
Аморфні сплави знаходяться в термодинамічно нерівноважному стані. В силу своєї аморфної природи металеві скла мають властивості, притаманні неметаллическим склі: при нагріванні в них проходять структурна релаксація, «расстекловиваніе» і кристалізація. Тому для стабільної роботи виробів з аморфних сплавів необхідно, щоб їх температура не перевищувала деякої заданої для кожного сплаву робочої температури.