Регуляція обміну таг
гормональна регуляція
Синтез і окислення триацилгліцеролів і жирних кислот залежить від співвідношення інсулін / глюкагон.
1. Зміна кількості ферментів
Ферменти комплексу пальмітатсінтази і ацетил-SКоА-карбоксилази є адаптивними ферментами, кількість їх зростає при посиленому харчуванні і зменшується при голодуванні і споживанні жиру. Індуктором біосинтезу цих ферментів є інсулін.
2. Ковалентний модифікація
Завдяки інсуліну, глюкагону, адреналіну, тиреотропному і адренокортикотропному гормонів відбувається ковалентная модифікація ферментів ацетил-SКоА-карбоксилази і ТАГ-ліпази шляхомфосфорилювання-дефосфорилирования.
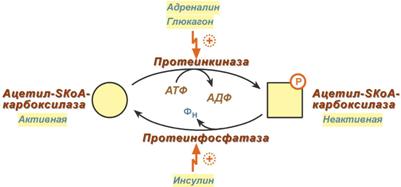
Регуляція активності ацетил-SКоА-карбоксилази
Інсулін активує протєїнфосфатаза і сприяє дефосфорілірованіе і активації ацетил-SКоА-карбоксилази. Одночасно в клітці дефосфорилюється і інактивується ТАГ-ліпаза.
Глюкагон. адреналін або інші гормони, діючи за аденілатціклазную механізму за участю цАМФ-залежної протеїнкінази, викликають фосфорилювання і інгібування ацетил-SКоА-карбоксилази і, отже, зупиняють липогенез. Одночасно вони активують ТАГ-липазу (механізм).
При зменшенні кількості інсуліну і зростанні глюкагону посилюються ліполіз в жировій тканині, надходження жирних кислот в печінку і інші тканини і реакції їх β-окислення. Такий стан спостерігається при гіпоглікемії будь-якого походження. При зворотному співвідношенні гормонів починаються реакції синтезу жирів.
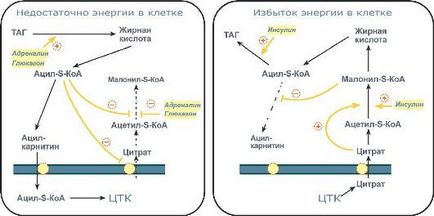
Способи регуляції реакцій обміну триацилгліцеролів
метаболічна регуляція
У регуляції синтезу і окислення жирних кислот відіграють роль три ділянки:
1. Активність ацетил-SКоА-карбоксилази регулюється:
- цитратом - аллостерічеський активатор ферменту, накопичується в цитоплазмі при надмірній кількості енергії,
- ацил-SКоА за принципом зворотного негативного зв'язку інгібує фермент, перешкоджаючи синтезу Малоні-SКоА. Тобто якщо ацил-SКоА не встигає вступити в етерифікацію або посилюється ліполіз в клітці або збільшується надходження жирних кислот ззовні, то автоматично блокується синтез нових жирних кислот.
2. Транспорт цитрату з мітохондрії в цитозоль пригнічується надлишком ацил-SКоА. це знижує синтез жирних кислот.
3. Карнітин-ацілтрансферази відзначено зниження при утворенні Малоні-SКоА. що зупиняє надходження ацил-SКоА всередину мітохондрій і знижує β-окислення.
Таким чином, коли в клітці є надлишок енергії. то посилення синтезу жирних кислот досягається надходженням в цитозоль цитрату і при наявності Малоні-S-КоА. Отримані молекули ацил-SКоА швидко надходять на етерифікацію гліцерину до ТАГ і не накопичуються в цитоплазмі.
Якщо в клітці недостатньо енергії. то необхідно активувати β-окислення жирних кислот для її отримання. В цьому випадку гормональні впливу викликають ліполіз (або надходження жирних кислот ззовні) і накопичення ацил-SКоА в цитоплазмі, що автоматично (див пункт 2) через зменшення кількості цитрату і Малоні-SКоА перешкоджає синтезу нових жирних кислот. Паралельно (див пункт 3) спад Малоні-SКоА і активація карнітин-ацил-трансферази запускає β-окислення.
Потрапила в мітохондрії жирна кислота неминуче окислюється до ацетил-SКоА.
При появі надлишку ацетильних груп і достатній кількості АТФ в мітохондріях печінки ці групи перенаправляються на синтез кетонових тіл.