Полум'я, продукти згоряння - студопедія
Простір, в якому розвивається пожежа, услов-но розділяється на три зони: горіння, теплового впливу і задимлення.
Зона горіння - частина простору, в якому про-тека процеси термічного розкладання або випаровування горючих рідин і матеріалів (твердих, рідких, газів, парів) в обсязі дифузійного факела і полум'я.
Зона теплового впливу примикає до зони горе-ня. У цій зоні протікають процеси теплообміну між поверхнею полум'я і горючими матеріалу-ми.
Зона задимлення - частина простору, примикаю-ного до зони горіння, в якому неможливе перебування людей без засобів захисту органів дихання і в якому важко ведення бойових дій під-розділень (див. Рис. 1.1).
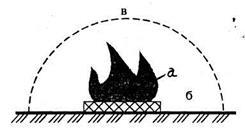
Мал. 1.1. Зони на пожежі: а - зона горіння; б - зона теплового впливу; в - зона задимлення;
Простір, в якому згорають пари і гази називається полум'ям або факелом. При уважному розгляді полум'я можна розрізнити три його зони (рис. 1.2). У нижній його частині 3 відбувається змішування газів, що утворюються з повітрям. Якщо швидко внести в цю частину полум'я голівку сірника і потримати її деякий час, то сірник спалахує не відразу. Отже, в цій частині полум'я температура невисока. Якщо в нижню частину полум'я внести скляну трубочку і до її отвору наблизити запалений сірник, то з'являється полум'я. Це доводить, що в ниж-ній частині полум'я є незгорілі гази. Середня частина полум'я 2является найяскравішою, оскільки тут під впливом щодо високої температури відбувається розкладання містять вуглець продуктів і частки вугілля сильно розжарюються і випромінюють світло. У зовнішній частині полум'я про-виходить повне згорання газів з утворенням оксиду вуглецю (IV) СО2 і води Н2 О. Слідом-ствие цього полум'я в цій частині, що не світяться. Описуючи полум'я, слід підкреслити, що багато його аспекти до цих пір залишаються недостатньо вивченими і ясними, уявлення про деякі з них досить суперечливі. Найбільш близькою до реальної інтерпретації феноменологических аспектів полум'я є висновок про те, що реакція в полум'я вуглеводнів починається задовго до світиться зони при порівняно невисоких температурах.
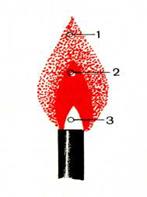
Мал. 1.2. будова полум'я
Полум'я може бути дифузійним або кінетичним. в залежності від того, чи горить заздалегідь приготована суміш парів або газів з повітрям або така суміш утворюється в полум'я в процесі горіння. В умовах пожежі горючі речовини: гази, рідини, тверді - горять дифузійним полум'ям.
За характером потоку розрізняють ламінарний і турбулентний диффузионное полум'я. При пожежах, як правило, утворюється турбулентний полум'я, але воно вивчено недостатньо, тому для пояснення цього явища використовуються положення теорії ламінарного полум'я.
Розглянемо будову дифузійного ламинарного полум'я рідини, що горить в посудині невеликого діаметра, а також газів і твердих речовин, якщо швидкість руху газів відповідає ламінарному режиму (див. Рис. 1.3).
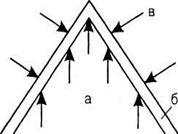
Мал. 1.3. Схема дифузійного ламинарного полум'я: а - зона горючих парів; б - зона горіння; в - навколишнє середовище (повітря)
Полум'я складається із зони горіння і зони парів. Зона горіння в дифузійному полум'ї є дуже тонкий шар, в якому протікає реакція горіння. Перетворення речовин і виділення тепла в цьому шарі викликає виникнення молекулярної дифузії в прилеглих до нього шарах повітря і пального. Причиною молекулярної дифузії є різниця парціальних тисків і температур газів, що беруть участь в горінні. Утворені в зоні горіння продукти дифундують як в повітря, так і в горючі пари. У полум'ї малого розміру продукти згоряння знаходяться у всьому обсязі зони парів, а в полум'ї великого розміру, тільки в шарі, прилеглому до зони горіння. Концентрація кисню в зоні горіння дорівнює нулю, так як він повністю вступає в реакцію. Внаслідок цього кисень не може дифундувати в зону парів і горіння в ній відсутня.
Відсутність зайвого кисню в зоні горіння викликає дифузію повітря в неї з навколишнього середовища, який, диффундируя через шар продуктів згоряння, втрачає частину кисню та азоту. Вступник в зону горіння кисень реагує з дифундують в неї пальним, а азот дифундує в зону утворення парів. Тому склад горючої суміші по фронту полум'я прагне до стехиометрическому. Температура полум'я змінюється по висоті зони горіння. Пояснюється це зміною складу стехиометрической суміші в зоні горіння і витратою тепла на нагрів надходить в неї повітря. У нижній частині полум'я, де утворюється стехіометрична суміш, яка повинна характеризуватися найбільшою теплотою горіння, температура горіння не є максимальною, тому що значна кількість тепла витрачається на нагрів холодного повітря. У середній частині полум'я теплота горіння суміші менше, ніж в нижній, що обумовлено дифузією в неї продуктів згоряння. Однак надходить в зону горіння нагріте повітря компенсує втрати тепла, і температура горіння в цій частині полум'я є максимальною. У верхній частині дифузійного полум'я горюча суміш має ще меншу теплоту горіння, і нагріте повітря, що надходить для утворення стехиометрической суміші не може компенсувати всіх втрат тепла, тому температура горіння тут мінімальна.
Колір полум'я залежить від термічної дисоціації парів біля зони нагріву. Атоми вуглецю, вступаючи в зону горіння, порушуються і, будучи деякий час у вільному стані, світяться. Якщо замість вуглецю вводити в полум'я солі міді, то воно забарвиться в зелений або синій кольори, якщо в полум'я потрапить сіль стронцію, то воно забарвиться в червоний колір. Так, за кольором полум'я і утворюється в деяких випадках сажі можна робити висновок про природу палаючих речовин і правильно вибрати огнетушащий склад.
За зовнішніми ознаками турбулентний полум'я відрізняється від ламінарного тим, що не має чітких обрисів і постійного положення фронту полум'я. Температура турбулентного полум'я завжди вище ламинарного.
Чудовою особливістю полум'я є його здатність мимовільно переміщатися по холодній горючої суміші. Це властивість характеризується нормальною швидкістю поширення полум'я (Uн), яка є єдиним параметром процесу горіння, що має властивість фізико-хімічної константи для конкретної горючої суміші. Сутність Uн схематично показана на рис. 1.4:
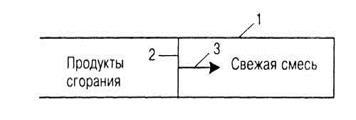
Мал. 1.4. Схема поширення полум'я в гомогенної газової суміші: 1 - скляна трубка, 2 - фронт полум'я, 3 - напрям поширення полум'я
У трубі приготовлена гомогенна горюча суміш. Якщо відкрити один її кінець (в даному випадку, лівий) і підпалити цю суміш у відкритого кінця, то виникає фронт полум'я, що переміщається в сторону свіжої суміші по нормалі до фронту полум'я. Гарячі продукти горіння будуть спливати в навколишнє середовище, і тому на фронт полум'я рівноваги вплив надаватися не буде. Якщо закрити і другий кінець труби, то скупчуються зліва від фронту полум'я продукти горіння, нагріті до максимальної температури горіння, будуть тиснути на фронт полум'я, викликаючи збільшення його швидкості. Ця швидкість, звана видимої швидкістю полум'я. Uв і визначається виразом:
де: Uв - видима швидкість полум'я, м / с;
Uн - нормальна швидкість поширення полум'я, м / с;
# 949; - ступінь розширення продуктів згоряння;
h - відношення числа молей продуктів згоряння до числа молей вихідної суміші (для вуглеводневих горючих речовин близька до одиниці);
Тг - температура горіння, К;
Т0 - початкова температура, К.
Для вуглецевих горючих сумішей Uн становить 0,30-0,45 м / с. Залежно від швидкості поширення полум'я горіння може бути дефлаграціонним (Uв до 10 м / с) і детонаційними (Uв приблизно від 10 3 м / с). Горіння при швидкості потужність між вищою дефлаграція і детонацією називають вибуховим. При швидкості Uв 60 м / с перед фронтом полум'я формується вибухова (ударна) хвиля. яка являє собою стрибкоподібне зміна тиску прилеглої до фронту середовища, що поширюється зі швидкістю, близькою до швидкості звуку. Тиск у фронті вибухової хвилі характеризує її руйнує здатність, але більш докладно це питання буде розглянуто в наступних темах.
При горінні речовин і матеріалів завжди утворюються продукти згоряння, це газоподібні, рідкі та тверді речовини, отримані в результаті з'єднання горючої з окислювачем (киснем повітря) в процесі горіння. Склад продуктів згоряння залежить від складу палаючого речовини і умов його горіння. При пожежі найчастіше горять органічні речовини (деревина, тканини, бензин, гас, гума та ін.), До складу яких входять головним чином вуглець, водень, кисень і азот. При їх горінні в достатній кількості повітря і при високій температурі горіння утворюються продукти повного згоряння: СО2. Н2 О, N2. При горінні в недостатній кількості повітря або при низькій температурі крім продуктів згоряння утворюються продукти неповного згоряння: СО, С (сажа). Відпрацьовані гази можуть бути вологими і сухими. Коли під час пожежі горять неорганічні речовини, такі як: сірка, фосфор, натрій, калій, алюміній, титан, магній і інші, продуктами їх згоряння в більшості випадків будуть тверді речовини: Na2 O2. CaO, MgO, P2 O5. Вони утворюються в дисперсному стані, тому піднімаються в повітря у вигляді щільного диму. Відпрацьовані гази алюмінію, титану та інших металів в процесі горіння знаходяться в розплавленому стані.
Дим являє собою дисперсну систему, що складається з найдрібніших твердих частинок в підвішеному стані в суміші продуктів згоряння з повітрям. Діаметр частинок диму під час пожежі коливається від 0,01 до 1 мкм. У складі диму, що утворюється при горінні органічних речовин, крім продуктів повного згоряння, містяться продукти термоокислительного розкладання горючих речовин. Вони утворюються при нагріванні ще не горять горючих речовин, що знаходяться в середовищі повітря або диму, що містить кисень. Зазвичай це відбувається перед факелом полум'я або у верхніх частинах приміщень, де знаходяться нагріті продукти згоряння.
Дим, що утворюється при пожежах, представляє велику небез-ність з наступних причин: висока температура; токсичність деяких продуктів горіння і термоокислительного розкладання, що входять до його складу, наприклад, HСN, CO, HC1, NO, NO2. СО2 та ін .; непрозорість диму, що знижує видимість і утрудняє дії людей під час пожежі; можливість утворення продуктами термоокислительного розкладання і неповного горіння, що входять до складу диму, вибухо-воопасних сумішей з повітрям.
Таким чином, небезпека диму обумовлюється як його дис-палої фазою, так і компонентами, що входять до його дисперсійне середовище. Так, дим, що виходить безпосередньо із зони реак-ції, може мати температуру понад 1000 0 С, а критичної тим-пература середовища, в якій людина може перебувати тривалий час, є температура 60 0 С.
Існує кілька способів боротьби з димом, що знижують його стійкість. До них відносяться використання розпорошених водяних струменів, при цьому знижується температура диму, збільшуючи його вологість, відбувається нейтралізація заряджених частинок, їх злипання існіженію агрегативной і кінетичної стійкості дисперсної системи (частки диму укрупнюються і осідають). Крім цього, боротьба з димом може здійснюватися шляхом його механічного видалення із задимлених приміщень за допомогою димососів або створенням природних конвективних потоків, наприклад, за допомогою димових люків.
Склад продуктів термоокислительного розкладання залежить від природи горючих речовин, температури і умов контакту з окислювачем. При термоокислювальну розкладанні горючих речовин, в молекулах яких містяться гідроксильні групи, завжди утворюється вода. Якщо до складу горючих речовин входить вуглець, водень, кисень, то продуктами термоокислительного розкладання є вуглеводні, спирти, альдегіди, кетони і органічні кислоти. Коли до складу горючих речовин, крім перерахованих елементів входитимуть хлор, азот, то в димі будуть хлористий і ціаністий водень, оксиди азоту та інші сполуки. Так, в димі при горінні капрону міститься ціаністий водень; при горінні лінолеуму «релін» - сірководень, діоксид сірки; при горінні органічного скла - оксиди азоту. Продукти неповного згоряння і термоокіслітелного розкладання в більшості випадків є токсичними речовинами, тому люди, що знаходяться в таких приміщеннях, отримують отруєння протягом досить короткого часу.