Плавлення твердих тіл - студопедія
Прикладом фазового переходу першого роду є плавлення та кристалізація твердих тіл. Процес плавлення грає важливу роль в природі (плавлення снігу і льоду на поверхні Землі, плавлення мінералів в її надрах і т.д.) і в техніці (виробництво металів і сплавів, лиття в форми та ін.).
Плавленіе- це процес переходу тіла з кристалічного твердого стану в рідке.
Головними характеристиками плавлення чистих речовин є температура плавлення (Тпл) і теплота (теплота плавлення Qпл), яка необхідна для здійснення процесу плавлення.
У процесі плавлення температура кристала залишається постійною. Ця температура і називається температурою плавлення Тпл. . У кожного речовини своя температура плавлення. Температура плавлення для даної речовини залежить від атмосферного тиску. Найвищу температуру плавлення серед чистих металів має вольфрам (3410 ° С), найнижчу -
ртуть (-38,9 ° С).
Сталість температури пояснюється тим, що при плавленні вся підводиться теплота йде на розупорядкування регулярного просторового розташування атомів (молекул) у кристалічній решітці. Для більшості кристалів (крім води, і деяких сплавів) температура плавлення зростає зі збільшенням зовнішнього тиску, так як для віддалення атомів один від одного при більшому тиску потрібна велика енергія теплових рухів, т. Е. Більш висока температура.
Розплавлене речовина володіє великим запасом внутрішньої енергії, ніж в твердому стані. Частина, що залишилася теплоти плавлення витрачається на здійснення роботи по зміні обсягу тіла при його плавленні. При плавленні обсяг більшості кристалічних тіл збільшується (на 3-6%), а при твердінні зменшується. Але, існують речовини, у яких при плавленні обсяг зменшується, а при твердінні - збільшується. До них відносяться, наприклад, вода і чавун, кремній і деякі інші. Саме тому лід плаває на поверхні води, а твердий чавун - у власному розплаві.
Плавлення починається при досягненні кристалічною речовиною Тпл. З початку плавлення до його завершення температура речовини залишається постійною і рівною Тпл, незважаючи на повідомлення речовини теплоти (рис. 1). Нагріти кристал до Т> Тпл в звичайних умовах не вдається, тоді як при кристалізації порівняно легко досягається значне переохолодження розплаву.
Плавлення відбувається з поглинанням прихованої теплоти фазового переходу - теплоти плавлення Qпл ..
Питома теплота плавлення qпл. показує, яка кількість теплоти необхідно для повного перетворення 1 кг речовини з твердого стану в рідке, взятого при температурі плавлення. qпл. = Qпл. / M, Дж / кг.
Плавлення супроводжується зміною фізичних властивостей речовини: збільшенням ентропії, що відображає розупорядкування кристалічної структури речовини; зростанням теплоємності, електричного опору. Практично до нуля падає при плавленні опір зрушенню, зменшується швидкість поширення звуку (подовжніх хвиль) і т.д.
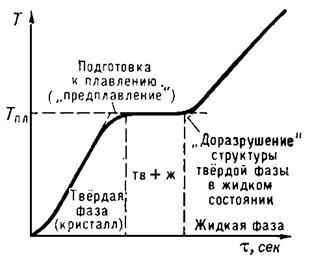
Мал. 1. Зупинка температури при плавленні кристалічного тіла.
По осі абсцис відкладено час # 964 ;, пропорційне рівномірно що підводиться до тіла кількості теплоти.
Згідно молекулярно-кінетичних уявлень, плавлення здійснюється наступним чином. При підведенні до кристалічного тіла теплоти збільшується енергія коливань (амплітуда коливань) його атомів, що призводить до підвищення температури тіла і сприяє утворенню в кристалі різного роду дефектів (незаповнених вузлів кристалічної решітки - вакансій; порушень періодичності грат атомами, що упровадилися між її вузлами, і ін . У молекулярних кристалах може відбуватися часткове розупорядкування взаємної орієнтації осей молекул, якщо молекули не володіють сферичної формою. Поступове зростання числа дефектів їх об'єднання характеризують стадію передплавлення. З досягненням Тпл в кристалі створюється критична концентрація дефектів, починається плавленіе- кристалічна решітка розпадається на легкорухливі субмикроскопические області. Подводимая при плавленні теплота йде не на нагрів тіла, а на розрив міжатомних зв'язків і руйнування далекого порядку в кристалах. В самих же субмикроскопических областях ближній порядок в розташуванні атомів при плавленні істотно не змінюється. Цим пояснюються менші значення теплот плавлення Qпл в порівнянні з теплотамі пароутворення і порівняно невелика зміна ряду фізичних властивостей речовин при їх плавленні. У міру зростання температури молекули рухаються все інтенсивніше. При нагріванні зростає не тільки молекулярно-кінетична енергія тіла, але і потенційна енергія взаємодії його атомів, оскільки при збільшенні амплітуди коливань атоми відходять один від одного на більшу відстань і зближуються на меншу відстань, завдяки чому енергія взаємодії їх електричних зарядів зростає. З підвищенням температури настає, нарешті, такий момент, коли підтримання порядку серед сильно розгойдуються атомів стає неможливим, і з цього моменту починається руйнування кристалічної решітки, в результаті чого зникає і дальній порядок. Тверде тіло плавиться.
У аморфних тіл зміна температури з часом не має ділянки з постійною температурою, а тільки точку перегину. Збільшення температури твердого аморфного тіла супроводжується безперервним зменшенням його в'язкості.
Зворотний перехід речовини в твердий стан можливий як з рідкого, так і з газоподібного стану. І в тому і в іншому випадку такий перехід здійснюється зі стану, позбавленого симетрії, в стан, в якому симетрія існує (це відноситься до дальнього порядку, який має місце в кристалах і якого немає ні в рідинах, ні в газах). Тому перехід в твердий стан повинен відбуватися стрибком при певній температурі, на відміну від переходу рідина-пар, який може відбуватися безперервно. Процес утворення твердого тіла при охолодженні рідини є процес утворення кристала (кристалізація) і відбувається він при певній температурі - температурі кристалізації. Так як при такому перетворенні енергія системи зменшується, то такий перехід повинен супроводжуватися виділенням енергії у вигляді теплоти кристалізації. Із закону збереження енергії випливає, що теплота плавлення і теплота кристалізації повинні бути рівні один одному.