Класична модель атома по Резерфорду
Моделі атома. 1903 року Дж. Дж. Томсон, запропонував модель атома, згідно з якою атом являє собою сферу, рівномірно заповнену позитивним електрикою. Електрони занурені в цю середу і взаємодіють з елементами цього середовища згідно із законом Кулона (рис. 4.1, а). Відповідно до цієї моделі атом в цілому нейтральний: сумарний заряд сфери і заряду електронів дорівнює нулю. Спектр такого атома повинен був бути складним, але аж ніяк не лінійчатим, що суперечило експериментальними даними. За моделлю Томсона коливається електрон (осцилятор) може випускати електромагнітну хвилю. При відхиленні електрона від положення рівноваги виникають сили, які прагнуть повернути його в положення рівноваги. Завдяки цьому виникають коливання електрона, які обумовлюють випромінювання атома.
Була запропонована також модель атома, зображена на рис. 4.1, б. атом складався зі сфери, в центрі якої знаходилося позитивно заряджене ядро, а навколо нього розташовувалися електрони. Однак і ця модель не змогла пояснити результати експериментів.
Найбільш відома планетарна модель атома, запропонована англійським фізиком Е. Резерфордом (рис. 4.1, в).
Перші експерименти з вивчення будови атома були виконані
Е. Резерфордом і його співробітниками Е.Марсденом і Х.Гейгером в 1909-1911 роках. Резерфорд запропонував застосувати зондування атома за допомогою # 945; частинок, які виникають при радіоактивному розпаді радію і деяких
інших елементів. Ці досліди стали можливі завдяки відкриттю явища радіоактивності, при якому в результаті природного радіоактивного розпаду важких елементів виділяються частинки, що мають позитивний заряд, рівний заряду двох електронів, маса частинки в 4 рази більша за масу атома водню, тобто вони є іонами атома гелію. Енергія частинок, що випускаються різними важкими хімічними елементами, змінюється від еВ для урану до еВ для торію. маса # 945; частинок приблизно в 7300 разів більше маси електрона, а позитивний заряд дорівнює подвоєному елементарному заряду. У цих дослідах використовувалися # 945; частинки з кінетичної енергією 5 МеВ. що відповідало їх швидкості близько м / с.
Ці частинки бомбардували фольги з важких металів (золото, срібло, мідь і ін.). Електрони, що входять до складу атомів, внаслідок малої маси не змінюють траєкторію # 945; частинки. Розсіювання, тобто зміна напрямку руху # 945; частинок, може викликати тільки важка позитивно заряджена частина атома.
Мета дослідів Резерфорда полягала в тому, щоб експериментально перевірити основні положення моделі атома, запропонованої Томсоном.
Схема досвіду Резерфорда по розсіюванню # 945; частинок показана на рис. 4.2.
Тут K - свинцевий контейнер з радіоактивною речовиною, Е - екран, покритий сірчистим цинком, Ф - золота фольга, M - мікроскоп. Від радіоактивного джерела, укладеного в свинцевий контейнер, # 945; частинки спрямовувалися на тонку металеву фольгу. Товщина фольги становила м (1 мкм), що еквівалентно приблизно 400 верствам з атомів золота. розсіяні фольгою # 945; частинки потрапляли на екран, покритий шаром кристалів сульфіду цинку, здатних світитися під ударами швидких заряджених частинок. Сцинтиляції (спалаху) на екрані спостерігалися оком
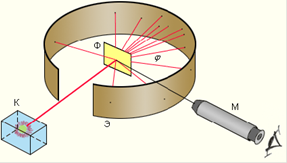
спостереження розсіяних # 945; частинок в досвіді Резерфорда можна було проводити під різними кутами # 966; до початкового напрямку пучка. Було виявлено, що більшість # 945; частинок проходило через тонкий шар металу, практично не відчуваючи відхилення. Однак невелика частина часток все ж відхилялася на значні кути, що перевищують 30 °. дуже рідкісні # 945; частинки (приблизно одна на десять тисяч) відчували відхилення на кути, близькі до 180 °. Цей результат був несподіваним, тому що знаходився в протиріччі з моделлю атома Томсона, згідно з якою позитивний заряд розподілений по всьому об'єму атома. При такому розподілі позитивний заряд не може створити сильне електричне поле, здатне відкинути # 945; частинки назад. Електричне поле однорідного зарядженого кулі максимально на його поверхні і убуває до нуля в міру наближення до центру кулі. Якби радіус кулі, в якому зосереджений весь позитивний заряд атома, зменшився в n раз, то максимальна сила відштовхування, що діє на # 945;-частинок за законом Кулона, зросла б у n 2 разів. Тоді при достатньо великому значенні n # 945; частинки могли б випробувати розсіювання на великі кути аж до 180 °. Ці міркування привели Резерфорда до висновку, що атом майже порожній, і весь його позитивний заряд зосереджений в малому обсязі, що має розміри близько
10 -14 м. Цю частину атома Резерфорд назвав атомнимядром. Електрони, на думку Резерфорда, рухаються навколо ядра з розмірами порядку 10 -14 м. Так виникла ядерна модель атома (рис. 4.1, в).
На підставі отриманих результатів Резерфорд, враховуючи, що електрони атома не можуть істотно впливати на розсіювання щодо важких і швидких частинок, зробив висновки, які були покладені в основу планетарної (ядерної) моделі атомів:
1) існує ядро, в якому зосереджена вся маса атома і весь його позитивний заряд, причому розміри ядра значно менше, ніж розмір самого атома;
2) електрони, які входять до складу атома, рухаються навколо ядра по кругових орбітах.
Виходячи з цих двох передумов і припускаючи, що взаємодія між налетающей -часткою і позитивно зарядженим ядром визначається кулоновскими силами, Резерфорд встановив, що атомні ядра мають розміри м. Тобто вони в раз менше розмірів атомів. Ядро займає лише 10 -12 частину повного обсягу атома, але містить весь позитивний заряд і не менш 99,95% його маси. Речовина, що становить ядро атома, має колосальну щільність # 961; ≈10 17 кг / м 3. Заряд ядра повинен бути дорівнює сумарному заряду всіх електронів, що входять до складу атома. Згодом вдалося встановити, що якщо заряд електрона прийняти за одиницю, то заряд ядра в точності дорівнює номеру цього елемента в таблиці Менделєєва. Величина позитивного електричного заряду атомного ядра Z визначається кількістю протонів в ядрі (і, отже, кількістю електронів в атомних оболонках), яке збігається з порядковим номером елемента в періодичній таблиці. Заряд дорівнює Zе. де е = 1,602 · 10 -19 Кл - абсолютна величина елементарного електричного заряду. Заряд визначає хімічні властивості всіх ізотопів даного елемента.
У 1911 Резерфорд, використовуючи закон Кулона, отримав формулу
де N - кількість # 945; частинок, що падають в одиницю часу на розсіювач; dN - кількість розсіяних в одиницю часу # 945; частинок в тілесному куті d # 937; під кутом # 952; ; Ze і n - заряд ядер розсіювача і їх концентрація; dx - товщина шару фольги; V і m # 945; -швидкість і маса # 945; частинок.
Прямі досліди з вимірювання заряду ядер на основі формули Резерфорда були виконані Чедвиком в 1920 році. Схема досвіду Чедвіка приведена на рис. 4.3.
Скло у вигляді кільця (заштрихована на рис. 4.3) розміщувався співвісно і на рівних відстанях між джерелом І і детектором # 945; частинок Д. При вимірюванні кількості dN розсіяних # 945; частинок отвір в кільці закривалося екраном, який поглинав прямий пучок # 945;-частинок з джерела
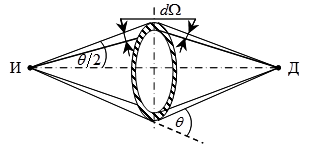
в детектор. Детектор реєстрував тільки # 945; частинки, розсіяні в тілесному
вугіллі d # 937; під кутом # 952; до падаючого пучку # 945; частинок. Потім кільце перекривався екраном з отвором, і вимірювалася щільність струму # 945; частинок в точці розташування детектора. За отриманими даними, розраховували кількість N # 945; частинок, що падають на кільце в одиницю часу. Таким чином, якщо відома енергія # 945; - частинок, що випускаються джерелом, без праці визначалася величина Z у формулі (4.1).
Формула Резерфорда дозволила пояснити експериментальні результати по розсіюванню # 945; частинок на важких ядрах. що призвело до відкриття атомного ядра і створення ядерної моделі атома.
Модель атома, запропонована Резерфордом, нагадує Сонячну систему. Саме тому модель Резерфорда одержала назву планетарної моделі атома. Ця модель стала значним кроком на шляху до сучасних уявлень про будову атома. Що лежить в її основі поняття атомного ядра, в якому зосереджені весь позитивний заряд атома і практично вся його маса, зберегло своє значення до теперішнього часу.
Однак, на відміну від планетарної моделі Сонячної системи, планетарна модель атома виявляється внутрішньо суперечливою з точки зору класичної фізики. І це, перш за все, пов'язано з наявністю у електрона заряду. Відповідно до законів класичної електродинаміки, що обертається навколо ядра електрон, як і будь-яка прискорено рухається заряджена частинка, буде випромінювати електромагнітні хвилі. Спектр такого випромінювання повинен бути безперервним, тобто містити електромагнітні хвилі з будь-якою довжиною хвилі. Уже цей висновок суперечить лінійного спектра випромінювання атомів, що спостерігається на досвіді.
Крім того, безперервне випромінювання зменшує кінетичну енергію електрона. Тому, за рахунок випромінювання радіус орбіти рухомого електрона зобов'язаний зменшуватися, і, врешті-решт, електрон повинен впасти на ядро, як показують оцінки, за час. Однак в дійсності атом водню є стійкою і «долгоживущей» електромеханічної системою. Іншими словами, планетарна модель атома з точки зору класичної фізики виявляється нестійкою.