Валентність хлору fecl2, felc3, то що цікаво!
Валентністю називається здатність елементів приєднувати до себе інші елементи.
Т. е. Валентність - це число, яке демонструє кількість елементів, яке може притягнути до себе конкретний атом. Визначається числом неспарених електронів незбудженого і збудженого атома.
Хлор, є елементом сьомої групи головною подругппи, третього періоду періодичної системи хімічних елементів Менделєєва. Атомний номер хлору - 17. Записується він як Cl від Chlorum. Хлор є активним неметаллом і входить до групи галогенів.
Валентність і ступінь окиснення атомів хлору в його молекулі

Ступінь окислювання чисельно позначається тим, в якому стані знаходиться атом в з'єднанні. Також її називають окислювальним числом. Визначаючи яке умовно вважають, що в простих ковалентних сполуках значення позитивної ступеня окислення елемента дорівнює кількості відтягнутих від атома зв'язують електронних пар, а значення негативної ступеня окислення - числом притягнутих електронних пар. Тому, визначаючи ступінь окислення прийнято вважати, що, з'єднання складаються тільки з позитивно і негативно заряджених іонів.
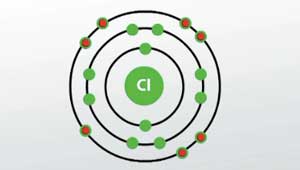
Говорячи про хлор, його валентності та ступені окислення в його молекулі, виходять такі значення:
- Валентність - 1.
- Ступінь окислення - 0
Яка валентність азоту фосфору кремнію
Яка ж валентність інших речовин, нерідко взаємодіючих з хлором?
- Валентність азоту. Азот в таблиці Менделєєва позначений буквою N. Він може істот овать в самому різному валентном вигляді залежачи від з'єднання. Зустрічається навіть дрібна валентність. Це можна прекрасно подивитися на прикладі окислення азоту: N2O - одновалентних азот (звеселяючий газ) NO - двовалентний. NO2 (діоксид азоту, бурий газ). Сполуки азоту в ступені окислення +5 - оксид азоту (V) N2O5, азотна кислота і її солі - нітрати, і ін.
Проте, валентність самого азоту = 3.
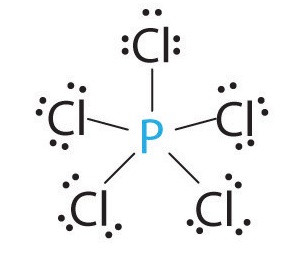
- Фосфор (Р) коштує в 3-му періоді, V групи, основною підгрупи періодичної системи Менделєєва. Валентність фосфору також може бути різною, все, як і з будь-яким іншим речовиною, впирається в те, з якою речовиною трапитися хімічний зв'язок фосфору. Проте валентність самогу фосфору буває III, V.
- Кремній (Si) - варто в 3 періоді, IV групі головної підгрупи періодичної системи. Валентність - 2, 4.
Валентність хлору в органічних сполуках, в збудженому стані, в хлороводню, у вищому оксиді
Валентність хлору в органічних сполуках може бути різною, залежно, власне, від з'єднання.
Основні реакції хлору з органічними речовинами:
- З насиченими сполуками:
CH3-CH3 + Cl2 → C2H5Cl + HCl
- Приєднується до ненасичених сполук за кратними зв'язками:
CH2 = CH2 + Cl2 → Cl-CH2-CH2-Cl
- Ароматичні сполуки заміщають атом водню на хлор в присутності каталізаторів (наприклад, AlCl3 або FeCl3):
C6H6 + Cl2 → C6H5Cl + HCl
У збудженому стані у атома хлору на 3 енергетичному рівні перебуває 1 неспарених електронів, таким чином збудженому атом хлору може показувати валентність 1.
У збудженому стані - валентність 3.
Вищим оксидом є оксид, де елемент проявляє вищу ступінь окислення.
Cl2O7 - оксид хлору (VII) - ст. оксиди. Cl (+7) - вищий оксид.
Валентність хлору з металами, з фосфором, з сріблом, з натрієм, з воднем, з киснем, з кальцієм, з алюмінієм, з неметалами, з залізом
Взагалі валентність - одна з найбільш складних тем в хімії, щоб в цьому розібратися, доведеться простудіювати чимало матеріалу. Не знаючи елементарних законів і правил хімії, ніхто не зможе зрозуміти, що ж таке валентність, а вже тим більше навчитися визначати її.
Взаємодія з металами:
Хлор безпосередньо вступає в реакцію практично з усіма металами, проте для реакції з деякими необхідна волога або нагрівання.
Взаємодія з неметалами:
C неметаллами (крім вуглецю, азоту, фтору, кисню і інертних газів), утворює відповідні хлориди.
У різних з'єднаннях валентність хлору також різниться, з металами (срібло, натрій, залізо, алюміній) валентність хлору = 1, з неметалами має різну валентність, але, найчастіше, також 1. У з'єднаннях з воднем валентність хлору = 1.
Взагалі CL завжди має валентність 1, з'єднуючись з речовинами, виключення складають речовини з валентністю VII.