Поведінка речовини в невагомості
Поведінка речовини в невагомості
Агрегатні і фазові стану речовини. При розгляді особливостей поведінки речовини в космічних умовах часто використовуються такі поняття, як агрегатний і фазовий стану, фаза і компоненти. Дамо визначення цих понять.
Агрегатні стани речовини розрізняються за характером теплового руху молекул або атомів. Зазвичай говорять про трьох агрегатних станах - газоподібному, твердому і рідкому. У газах молекули майже не пов'язані силами тяжіння і рухаються вільно, заповнюючи весь посудину. Структура кристалічних твердих тіл характеризується високою впорядкованістю - атоми розташовані в вузлах кристалічної решітки, біля яких вони здійснюють лише теплові коливання. В результаті кристалічні тіла мають строго обмежену форму, а при спробі якимось чином змінити її виникають значні пружні сили, які протидіють такій зміні.
Поряд з кристалами відома й інша різновид твердих тіл - аморфні тіла. Головна особливість внутрішньої будови аморфних твердих тіл - відсутність повної впорядкованості: лише в розташуванні сусідніх атомів дотримується порядок, який змінюється хаотичним розташуванням їх один щодо одного на більш значних відстанях. Найбільш важливий приклад аморфного стану - це скло.
Тим же самим властивістю - ближнього порядку в розташуванні сусідніх атомів - володіє речовина в рідкому агрегатному стані. З цієї причини зміна обсягу рідини не викликає в ній виникнення значних пружних сил, і в звичайних умовах рідина приймає форму судини, в якому вона знаходиться.
Якщо речовина складається з декількох компонентів (хімічних елементів або сполук), то його властивості залежать від відносної концентрації цих компонентів, а також від температури, тиску та інших параметрів. Для характеристики кінцевого продукту, що утворюється при такому комбінуванні компонентів, використовується поняття фази. Якщо розглядається речовина складається з межують один з одним однорідних частин, фізичні або хімічні властивості яких різні, то такі частини називаються фазами. Наприклад, суміш льоду і води являє собою двофазну систему, а вода, в якій розчинений повітря, - однофазную, тому що в цьому випадку відсутній межа розділу між компонентами.
Фазовий стан - поняття, засноване на структурному поданні терміна «фаза». Фазовий стан речовини визначається тільки характером взаємного розташування атомів або молекул, а не їх відносним рухом. Наявність далекого порядку (повна упорядкованість) відповідає кристалічному фазовому стану, близького порядку - аморфному фазового стану, повна відсутність порядку - газоподібному фазовому стану.
Фазовий стан не обов'язково збігається з агрегатним. Наприклад, аморфному фазового стану відповідає звичайне рідке агрегатний стан і тверде склоподібний стан. Твердому агрегатному стані відповідають два фазових - кристалічний і аморфний (склоподібний).
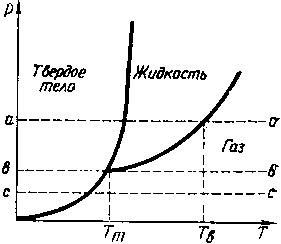
Мал. 2. Діаграммар-Травновесія однокомпонентной системи
Перехід речовини з одного фазового стану в інше називається фазовим переходом, або перетворенням. Якщо дві або більше різних фаз речовини при даній температурі і тиску існують одночасно, стикаючись один з одним, то говорять про фазовий рівновазі. На рис. 2 як приклад приведена діаграма фазового рівноваги однокомпонентной системи, побудована в координатах тиск (р) - температура (T). Тут ізобара (т. Е. Пряма постійного тиску) а-а відповідає прямим переходах тверде тіло - рідина (плавлення і затвердіння) і рідина - газ (випаровування і конденсація), ізобара с-с - переходу тверде тіло - газ (сублімація), а ізобара в-в - співіснування всіх трьох фаз в так званій потрійний точці, при певних значеннях р і Т.
Вплив невагомості на рідину. Як впливає тяжіння на поведінку речовини в різних агрегатних станах? У твердих тілах атоми і молекули розташовуються в строго визначеному порядку, і сила тяжіння не може істотно впливати на процеси, що відбуваються в цьому стані.
На процеси в газах ця сила може вплинути більш значно. Відомо, наприклад, що в умовах нерівномірного нагрівання різних верств газу в атмосфері виникає під дією сили тяжіння вільна конвекція, т. Е. Упорядкований обмін газу між цими шарами. В умовах невагомості цей ефект може не виникнути.
Але особливо сильний вплив сила тяжіння надає на рідину. При переході до невагомості в рідини зникає сила Архімеда, яка діє на компоненти різної щільності і яка веде до їх поділу, змінюється характер конвекційних течій, зростає відносна роль міжмолекулярних взаємодій в рідини і стає можливим її вільне утримання поза судини (явище левітації). Розглянемо з цих причин докладніше процеси, що відбуваються в рідині.
Як і в газі, в рідині молекули незберігають постійного положення, а за рахунок теплової енергії переміщуються з місця на місце. Якщо в будь-якому місці рідини переважають частки одного сорту, то за рахунок більш частих зіткнень між собою вони поступово переходять в зону, де їх концентрація менше. Цей процес називається дифузією. Внаслідок дифузії за час t відбувається зміщення частинок на відстань х = (2Dt) 1/2. де D - коефіцієнт дифузії. Якщо розглядати частки як сфери з радіусом r. то D = W · (?? r) -1. Тут W - теплова енергія частинок. - в'язкість рідини, яка сильно залежить від її температури. Коли рідина охолоджується, то в'язкість зростає і відповідно сповільнюються процеси дифузії.
Якщо зміна концентрації частинок одного сорту на відстані? X всередині рідини дорівнює? С. то через одиничну площадку в 1 з має проходити число частинок I = - D? c /? x.
У деяких випадках рідина може містити компоненти різної щільності. На Землі під дією сили Архімеда поступово відбувається поділ цих компонентів (наприклад, з молока утворюються вершки і обрат). В невагомості цього поділу немає, і після затвердіння таких рідин можуть бути отримані речовини з унікальними властивостями. Рідина може також містити фази, які не змішуються між собою, наприклад, гас і воду. На Землі між ними утворюються чіткі межі розділу. В невагомості шляхом перемішування можна отримати стійку суміш, що складається з дрібних крапель тієї та іншої фаз. Після затвердіння з подібних сумішей різних фаз можна отримати однорідні композиційні матеріали, пенометалли і т. П.
Виникнення кордонів розділу між різними фазами в рідини пов'язано з наявністю сили поверхневого натягу, або капілярної сили, яка виникає через взаємодію між молекулами рідини. Поверхневий натяг можна уподібнити силі, яка повертає в початковий стан струну, коли музикант намагається відтягнути її в сторону. Саме сила поверхневого натягу призводить до того, що з погано закритого крана падають краплі, а не ллється тоненька цівка води. Але на Землі ці краплі невеликі: сила тяжіння багато більше сил поверхневого натягу і розриває на частини занадто великі з них. В невагомості ніщо не може перешкоджати утворенню досить великих крапель, і рідке тіло, надане саме собі, буде приймати сферичну форму.
Насправді на борту космічного апарату через різного роду малих прискорень стан невагомості порушується. Якщо r - радіус сфери, форму якої приймає рідина, то діюча на неї капілярна сила приблизно дорівнює? R. де. - коефіцієнт поверхневого натягу. Величина інерційних масових сил, що діють на рідину, дорівнює? Gr 3. де. - щільність рідини, g - мале прискорення. Очевидно, ефекти поверхневого натягу будуть відігравати головну роль, коли. · (? Gr 2) -1> 1. Цим умовою визначається можливість отримання в стані, близькому до невагомості, рідких сфер з радіусом r. Такі рідкі сфери на борту космічних апаратів можуть перебувати в вільно плаваючому стані, коли для їх утримання не потрібні судини. Якщо це рідкий розплав, то при його затвердінні на Землі зі стінок посудини надходять шкідливі домішки. У космосі можна обійтися без судини і, отже, отримувати більш чисті речовини.
Тепло- і масообмін в невагомості. Істотний вплив перехід до невагомості надає також на процеси тепло- і массобмена в рідинах і газах. Перенесення тепла може здійснюватися теплопровідністю, конвекцією або випромінюванням, а також будь-яким поєднанням цих механізмів. Теплопровідність - це процес перенесення тепла із зони з більш високою температурою в зону, де температура нижче, шляхом дифузії молекул середовища між цими зонами. З цієї причини коефіцієнт теплопровідності пропорційний коефіцієнту дифузії.
Теплообмін випромінюванням характерний головним чином для твердих і рідких тіл і відбувається при досить високих температурах. Процеси променистого теплообміну і теплопровідності не залежать ні від сили тяжіння, ні від малих масових сил, що діють на борту космічних апаратів.
Інша річ конвективний теплообмін. Конвекція - це перенесення тепла в рідкому або газоподібному середовищі шляхом макроскопічного переміщення речовини цього середовища. Вище вже наводився найпростіший приклад конвекції - вільна (або природна) конвекція, що виникає внаслідок нерівномірного розподілу температури в середовищі, підданого дії масових сил (наприклад, сили тяжіння або інерційних сил, викликаних малими прискореннями на борту космічного апарату). Це явище кожен може легко спостерігати у себе вдома в будь-яких кип'ятильниках, коли шари рідини, які мають більш високу температуру і внаслідок цього більш низьку щільність, будуть спливати вгору і переносити з собою теплоту, а на їх місце, на гаряче дно кип'ятильника, будуть опускатися більш холодні і щільні шари.
Відносна роль теплообміну за рахунок вільної конвекції і теплопровідності визначається числом Релея:
Тут g - чинне на систему прискорення, L - характерний розмір системи. - коефіцієнт об'ємного розширення,? T - перепад температури в середовищі. - коефіцієнт теплопровідності. - в'язкість середовища. Звідси випливає, що в умовах, що наближаються до невагомості (g> 0), Ra> 0, і, отже, роллю конвекції, що веде до ефективного перемішування середовища, можна знехтувати.
Цей висновок має двояке значення. По-перше, зменшується внесок конвекції в процеси теплообміну, і передача тепла здійснюється більш повільним процесом теплопровідності. По-друге, виключення конвекційних струмів в середовищі призводить до того, що основну роль в масообмінних гратимуть не макроскопічні переміщення речовини, а процеси дифузії. А це, в свою чергу, відкриває можливість отримання речовин, розподіл домішок в яких буде значно більш однорідним, ніж на Землі.
Крім вільної конвекції, існує цілий ряд Інших конвекційних ефектів, одна частина яких залежить від масових сил, а інша ні. Відома також вимушена конвекція, яка відбувається під дією якого-небудь зовнішнього фактора (наприклад, мішалки, насоса і т. П.). В космічних умовах цей вид конвекції використовують, щоб забезпечити потрібну швидкість відводу тепла від працюючих агрегатів.
Як приклад конвекції, що не залежить від масових сил, вкажемо термокапіллярную конвекцію, яка виражається в тому, що на кордоні рідкої фази можуть виникати і поширюватися хвилі. Капілярні хвилі обумовлені перепадами температури, через наявність яких величина коефіцієнта поверхневого натягу непостійна уздовж поверхні. Цей тип конвекційного течії, очевидно, не залежить від величини g і може призводити до погіршення однорідності матеріалів, отриманих в космічних умовах. Спосіб компенсації шкідливих наслідків цього ефекту полягає в зменшенні фактичних перепадів температури уздовж поверхні розділу фаз.