Поняття про аерозолях, суспензіях і емульсіях
Аерозолі. Аерозолями називають вільно-дисперсні системи з газоподібної дисперсним середовищем і дисперсною фазою, що складається з твердих або рідких частинок. Аерозолі утворюються при вибухах, дробленні і розпилюванні речовин, а також в процесах конденсації при охолодженні пересичених парів води і органічних рідин. Аерозолі можна отримати і за допомогою хімічних реакцій, що протікають у газовій фазі.
По агрегатному стані частинок аерозолі класифікують на тумани (ж / б) - дисперсна система складається з крапельок рідини, дими (т / г) - аерозолі з твердими частинками конденсаційного походження, пилу (т / г) - тверді частинки, утворені шляхом диспергування. Можливі системи змішаного типу, коли на твердих частинках конденсується волога. Так виникає «зміг» - туман, що утворився на частинках диму.
Найбільш високодисперсними аерозолями є дими, розміри твердих частинок яких знаходяться в межах 10 -9 - 10 -5 м; частинки пилу мають розміри понад 10 -5 м, розміри крапельок туманів від 10-7 до 10 -5 м.
Особливості аерозолів полягає в тому, що через низьку в'язкості повітря седиментация і дифузія частинок аерозолю протікає дуже швидко. Крім того тумани і дими дуже легко переносяться вітром, що використовують для створення димових завіс, обкурювання і обприскування сільськогосподарських культур. Електричні властивості аерозолів дуже сильно відрізняються від електричних властивостей систем з рідким середовищем, що пояснюється різким розходженням щільності і діелектричних властивостей газів і рідин. У газовому середовищі відсутні електролітична дисоціація і ДЕС. Однак частинки в аерозолях мають електричні заряди, які виникають при випадкових зіткненнях часток один з одним або з якою-небудь поверхнею. Можлива також адсорбція іонів, що утворюються при іонізації газів під дією космічних, ультрафіолетових і радіоактивних випромінювань. Для аерозолів характерна крайня Агрегативна нестійкість. Їх тривале існування пов'язане з високою дисперсністю і малою концентрацією. Це означає, що стійкість аерозолів є лише кінетичної, термодинамічні фактори стійкості відсутні.
Як і будь-які дисперсійні системи, аерозолі утворюються двома методами - конденсаційним і диспергационними. До конденсаційному методу відносяться виникнення туману при охолодженні насиченого пара.
При диспергационними методах отримання аерозолів тверді або рідкі тіла роздрібнюють зазвичай механічним шляхом, а потім тверді частинки або рідкі крапельки розподіляються в газі. Наприклад, пневматичне розпилення рідин здійснюється за допомогою аерозольних балончиків при отриманні парфюмерно-косметичних аерозолів, аерозолів інсектицидів, емалей.
Для аерозолів характерні специфічні процеси, пов'язані з їх кінетичними властивостями: термофорез, фотофорез і термопреципітації. Явище термофорез полягає в русі частинок в напрямку зниження температури. Це пояснюється тим, що більш нагріту сторону частки молекули газу бомбардують з більшою швидкістю, ніж менш нагріту. Фотофорез полягає в пересуванні частинок при односторонньому їх освітленні. Термофорез і фотофорез мають велике значення в русі атмосферних аерозолів, наприклад при утворенні хмар.
Термопреципітації є осадження частинок аерозолю на холодних поверхнях за рахунок втрати частинками кінетичної енергії. Цим пояснюється осадження пилу на стінах і стелі близько обігрівальних приладів.
Роль аерозолів в природі, промисловості і побуті надзвичайно велика. Наприклад, вплив облікової і туманів на клімат, перенесення вітром насіння і пилку рослин, пневматичні способи забарвлення і покриття поверхонь розпорошеними металами, застосування розпорошеного палива, внесення добрив.
Аерозолі знайшли широке застосування в медицині і фармації. Стерильні аерозолі в спеціальних упаковках типу балонів застосовуються для стерилізації операційного поля, ран, опіків; інгаляційні аерозолі, що містять антибіотики і інші лікарські речовини, застосовують для лікування дихальних шляхів; аерозолі локального застосування використовують замість перев'язувальних засобів; аерозолі у вигляді клею застосовують у хірургічній практиці для склеювання ран, шкіри, бронхів, судин і т.д.
Суспензії. Суспензії - дуже поширені мікрогетерогенні системи з рідким середовищем твердої і твердої дисперсної фазою з розмірами частинок вище, ніж в колоїдних системах, т.зв. в діапазоні 10 -6 - 10 -4 м. Найбільш Грубодисперсні системи називають металевий порошок. До них відносяться глинисті, цементні і вапняні «розчини», олійні фарби.
Відрізняючись від ліофобних колоїдів в основному тільки більш низьким ступенем дисперсності, суспензії, в принципі, можуть бути отримані як конденсаційними, так і диспергационними методами. Однак на практиці їх отримують шляхом диспергування нерозчинних твердих речовин в рідкому середовищі або взмучіванія в цьому середовищі попередньо отриманого порошку.
Завдяки низького ступеня дисперсності в суспензіях слабо проявляються або відсутнє таке молекулярно-кінетичне властивість, як броунівський рух, а значить і дифузія. Осмотичний тиск, дуже слабо виражене в ліофобних колоїдах, в суспензіях практично не виявляється, так як часткова концентрація в них ще менше, ніж в лоіфобних колоїдах. В'язкість розбавлених суспензій мало відрізняється від в'язкості дисперсійного середовища. Висококонцентровані суспензії (пасти) мають властивості структурованих систем і характеризуються високою в'язкістю.
Суспензії не виявляють светорассеяния, і до них непридатний закон Релея, так як розмір частинок в суспензіях виключає можливість дифракції.
Внаслідок низького ступеня дисперсності суспензії є кінетично нестійкі системами (вони легко седіментіруются), а для досягнення агрегативной стійкості необхідно виконання принаймні однієї з двох умов: 1) смачиваемость поверхні частинок дисперсної фази дисперсної середовищем; 2) наявність стабілізатора. Додається стабілізатор вводять у вигляді поверхнево-активних речовин, або у вигляді високомолекулярного з'єднання. Якщо стабілізатор відсутня, але частинки суспензії добре змочуються дисперсійним середовищем, то на їх поверхні утворюється сольватна оболонка, що володіє пружними властивостями і перешкоджає з'єднанню частинок в крупні агрегати.
Емульсії. Емульсії - система, що складається з двох рідких фаз, одна з яких дисперговані у вигляді крапельок в інший. Рідина, роздроблена на крапельки, називається дисперсною фазою, а рідина, що заповнює об'єм між крапельками, - дисперсійним середовищем. Для існування стійкої емульсії необхідно, щоб рідини, що утворюють емульсію, була практично взаємно нерозчинні або мали досить малою розчинністю. Розмір частинок дисперсної фази емульсій коливається в межах від 10 -7 до 10 -5 м, і тому їх можна віднести до мікрогетерогенних системам.
Характерною рисою емульсій є те, що в залежності від умов виникнення будь-яка з двох рідин, що утворюють дисперсионную систему, може виявитися як дисперсною фазою, так і дисперсійним середовищем. Найчастіший випадок - емульсія води (В) і нерозчинної в ній органічної рідини (наприклад масло, бензол, хлороформ), яку умовно називають маслом (М). Можливі два типи таких емульсій: емульсії в яких дисперсійним середовищем є олія, і емульсії з водою дисперсною фазою. Перший тип емульсій називають емульсією масла у воді (скорочено М / В) або емульсіями першого роду (прямі). Другий тип - емульсії води в олії (В / М) або емульсії другого роду (зворотні).
Емульсії отримують методом механічного диспергування, хоча, в принципі, можливе використання і методів конденсації. Для диспергування qпріменяют різні мішалки, змішувачі, гомогенізатори, колоїдні млини. Високодисперсні емульсії часто отримують способом ультразвукового диспергування.
Емульсії є седиментаційно нестійкими системами. Якщо дисперсна фаза і дисперсійне середовище відрізняються по щільності, то можлива седиментация (або спливання) крапель дисперсної фази, тобто порушення однорідності концентрації. Агрегативна нестійкість емульсій проявляється в мимовільному злиття крапельок в дисперсної фазі - коалесценція. Цей процес може привести до руйнування емульсії і поділу її на два рідких шару.
Емульсії, як і всі мікрогетерогенні системи, володіють великою поверхнею розділу фаз. Освіта поверхні розділу завжди вимагає роботи, і робота ця тим більше, чим вище поверхневий натяг на цій поверхні. Тому легке утворення емульсії і підвищення її стійкості забезпечуються введенням речовин, які адсорбируясь на кордоні розділу фаз, зменшують поверхневий натяг на ній. Такі речовини називаються емульгаторами.
Поряд зі зниженням поверхневого натягу емульгатори можуть стабілізувати емульсію також і тим, що на поверхні розділу утворюється компактна плівка з емульгатора, що володіє відомою механічною міцністю. Такі плівки захищають частинки емульсії від коалесценції. На відміну від суспензій цей фактор може бути більш важливим, ніж створення на поверхні крапельок електричних зарядів.
Розглянемо докладніше механізм емульгування на прикладі емульгатора в емульсії М / В. Полярні (дифільні) молекули емульгатора (рис.7, глава 13) адсорбуються на поверхні крапельки масла, розчиняючись неполярними радикалами в маслі, а полярними групами в воді. В результаті адсорбції емульгатора поверхневий натяг краплі олії знижується, значить, значення поверхневої енергії зменшується. В результаті система стає стійкішим. Крім того, що утворюється гидратная клітина міцно зв'яже крапельки масла з дисперсійним середовищем (в даному випадку з водою), що буде перешкоджати коалесценции.
Якщо в якості емульгатора використовують молекули, здатні до дисоціації на іони (наприклад, мило, що представляє собою суміш жирних кислот), то крапелька масла зарядиться негативно, що призведе до ще більшої стабільності емульсії.
Як емульгатори можуть бути використані і тверді речовини, що застосовуються у вигляді порошку. У цьому випадку механізм емульгування пов'язаний зі смачиваемостью порошку рідиною, що входить до складу емульсії, і з освітою навколо крапельок твердих міцних оболонок. Гідрофільні емульгатори, такі, як глина, крейда, гіпс, стабілізує емульсії типу М / В, а гідрофобні (порошок сажі) - емульсії типу В / М.
Специфічним властивістю більшості емульсій є взаємне перетворення емульсій двох типів:
Цей процес, який отримав назву звернення фаз. призводить до того, що дисперсна фаза даної емульсії стає дисперсійним середовищем новоствореної системи, а дисперсійне середовище даної емульсії - дисперсною фазою новоствореної емульсії. Здійснюється це введенням поверхнево-активної речовини, яке стабілізує зворотний тип емульсії. Наприклад, емульсію типу М / В, стабілізовану олеатом натрію, переводять в емульсію В / М введенням надлишку олеата кальцію. Емульсію бензолу у воді, стабілізовану милом лужного металу, перетворюють в емульсію води в бензолі додатком до неї при струшуванні невеликої маси хлориду кальцію. Утворюється при цьому кальцієва сіль мила, добре розчинна у бензолі, стабілізує емульсію води в бензолі.
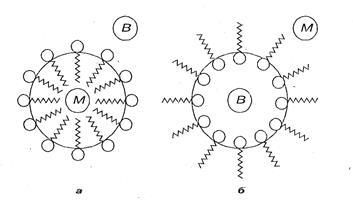
Рис 7 Звернення емульсій
Біологічне значення емульсій дуже велике. Наприклад, молоко і яєчний білок являє собою емульсії типу М / В. Засвоєння жирів в організмі здійснюється через їх емульгування під впливом жовчі. Молочний сік каучуконосних рослин (латекс) також є емульсією. Емульсії знаходять широке застосування в промисловості: бітумні емульсії для асфальтування, фарби, «ріжучі емульсії», використовувані при обробці металів.
Значення суспензій, емульсій і суспензій у фармації полягає в тому, що вони входять в обов'язковий асортимент ліків, що випускаються як за заводською технологією, так і з аптечної технології. До них відносяться альбіхоловая і нафталановая, масляні емульсії, емульсії для внутрішнього застосування; суспензії - лініменти синтомициновую, Стрептоцидова, новоціллін і ін .; суспензії ліофільних набухають речовин (танальбин) і ліофобних речовин (камфори, фенілсаліцилату, ментолу, сірки і до.), пінні препарати проти запалення шкірних покривів, опіків тощо