Молекулярно-кінетична теорія ідеальних газів
Молекулярно-кінетичної теорії ІДЕАЛЬНИХ газів
Сторінка 1 з 3
2. Основи молекулярної фізики і термодинаміки
2. Визначте число N атомів в 1 кг водню і масу одного атома водню.

3. У закритій посудині місткістю 20 л знаходяться водень масою 6 г і гелій масою 12 г. Визначте: 1) тиск; 2) молярну масу газової суміші в посудині, якщо температура суміші Т = 300 К.

4. Визначте щільність суміші газів водню масою m1 = 8 г і кисню m2 = 64 г при температурі Т = 290 К і при тиску 0,1 МПа. Гази вважати ідеальними.

5. У балоні місткістю 15 л знаходиться азот під тиском 100 кПа при температурі t1 = 27 ° С. Після того як з балона випустили азот масою 14 г, температура газу стала рівною t2 = 17 ° С. Визначте тиск азоту, що залишився в балоні.
6. Балон місткістю V = 20 л містить суміш водню і азоту при температурі 290 К і тиску 1 МПа. Визначте масу водню, якщо маса суміші дорівнює 150 м
7. Азот масою 7 г перебуває під тиском p = 0,1 МПа і температурі Т1 = 290 К. Внаслідок ізобарного нагрівання азот зайняв об'єм V2 = 10 л. Визначте: 1) обсяг газу до розширення, 2) температуру газу після розширення, 2) щільність газу до і після розширення.

8. У посудині місткістю 1 л знаходиться кисень масою 1 г. Визначте концентрацію молекул кисню в посудині.
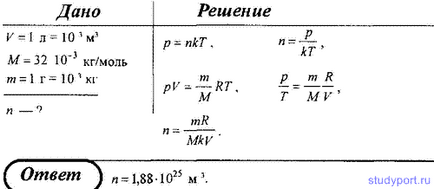
9. У посудині місткістю 5 л при нормальних умовах знаходиться азот. Визначте: 1) кількість речовини v; 2) масу азоту; 3) концентрацію n його молекул в посудині.
10. Середня квадратична швидкість деякого газу при нормальних умовах дорівнює 480 м / с. Скільки молекул містить 1 г цього газу?

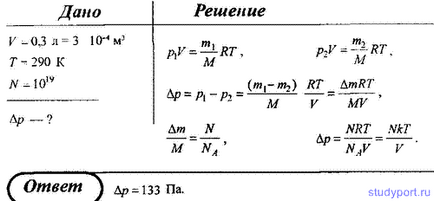
11. У посудині місткістю V = 0.3 л при температурі Т = 290 К знаходиться деякий газ. Наскільки знизиться тиск газу в посудині, якщо з нього через витік вийде N = 10 19 молекул.
12. Визначте тиск, який чиниться газом на стінки посудини, якщо його щільність ρ = 0,01 кг / м 3 і середня квадратична швидкість молекул газу становить 480 м / с.

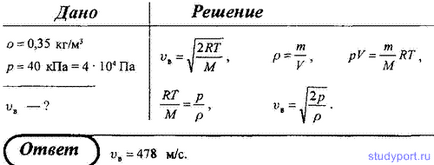
13. Визначте найбільш ймовірну швидкість молекул газу, густина якого при тиску 40 кПа становить 0,35 кг / м 3.
14. Визначте середню кінетичну енергію (ε0) поступального руху молекул газу, що заходять під тиском 0,1 Па і мають концентрацію молекул 10 13 см -3.

15. Визначте: 1) найбільш ймовірну vв; 2) середню арифметичну v; 3) середню квадратичну vкв швидкість молекул азоту (N2) при 27 ° С.
16. При якій температурі середня квадратична швидкість молекул кисню більше їх найбільш вірогідною швидкості на 100 м / с?

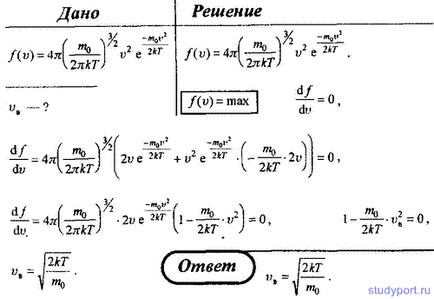
17. Використовуючи закон розподілу молекул ідеального газу за швидкостями, знайдіть формулу найбільш вірогідною швидкості Vв.
18. Використовуючи закон розподілу молекул ідеального газу за швидкостями, знайдіть закон, що виражає розподіл молекул за відносними швидкостями u (u = v / vв).

19. Використовуючи закон розподілу молекул ідеального газу за швидкостями, знайдіть середню арифметичну швидкість v молекул.
Вказівка: середня арифметична швидкість визначається за формулою
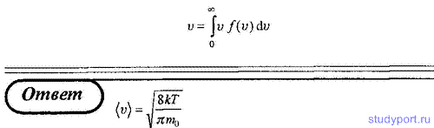
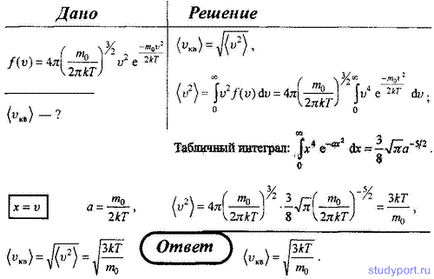
20. Використовуючи закон розподілу молекул ідеального газу за швидкостями, знайдіть середню квадратичну швидкість (vкв).
Молекулярно-кінетичної теорії ІДЕАЛЬНИХ газів - СТОРІНКА 2
Сторінка 2 з 3
21. Використовуючи функцію розподілу молекул ідеального газу по енергіях, знайдіть середню кінетичну енергію (ε) молекул.

22. Використовуючи функцію розподілу молекул ідеального газу по енергіях, знайдіть найбільш ймовірне значення енергії εв молекул.

23. Використовуючи функцію розподілу молекул ідеального газу по енергіях, знайдіть для даної температури відношення середньої кінетичної енергії ε молекул до їх найбільш вірогідного значення енергії εв.

24. Закон розподілу молекул газу за швидкостями в деякому молекулярному пучку має вигляд f (v) = Av 3 e -m0v ^ 2. визначте: 1) найбільш ймовірну швидкість; 2) найбільш ймовірне значення енергії молекул в цьому пучку.

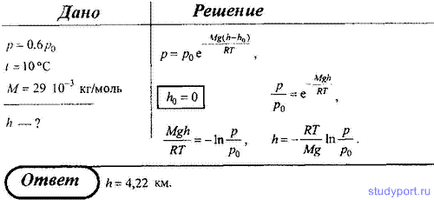
25. На якій висоті тиск повітря становить 60% від тиску на рівні моря? При вирішенні вважати, що температура повітря скрізь однакова і дорівнює 10 C.
26. Яке тиск повітря в шахті на глибині 1 км, якщо вважати, що температура по всій висоті постійна і дорівнює 22 С, а прискорення вільного падіння не залежить від висоти? Тиск повітря біля поверхні Землі одно p0.

27. Визначте відношення тиску повітря на висоті 1 км до тиску на дні свердловини глибиною 1км. Повітря у поверхні Землі знаходиться при нормальних умовах, і його температура не залежить від висоти.

28. На якій висоті щільність повітря в е раз (е - основа натуральних логарифмів) менше в порівнянні з його щільністю на рівні моря? Температуру повітря і прискорення вільного падіння вважайте незалежними від висоти.
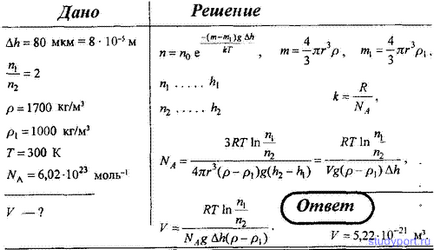
29. Використовуючи ідею установки Перрена для визначення постійної Авогадро і застосувавши до частинкам фарби, зваженим у воді, больцманівського розподіл, знайдіть обсяг частинок, якщо при відстані між двома шарами 80 мкм число зважених часток в одному шарі вдвічі більше, ніж в іншому. Щільність розчиненої фарби 1700 кг / м 3. а температура навколишнього середовища 300 К.
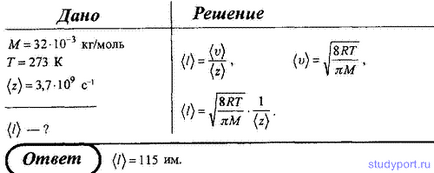
30. Визначте середню довжину вільного пробігу l молекул кисню, що знаходиться при температурі 0 С, якщо відомо середнє число z зіткнень, які долають молекулою за 1 с, одно 3,7 * 10 9.
31. При якому тиску середня довжина вільного пробігу молекул водню дорівнює 2,5 см, якщо температура газу дорівнює 67 С? Діаметр молекули водню вважати рівним 0,28 нм.

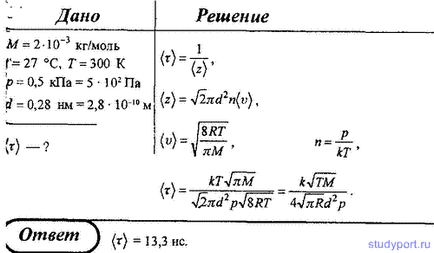
32. Визначте середню тривалість τ вільного пробігу молекул водню при температурі 27 С і тиску 0,5 кПа, приймаючи діаметр молекули водню рівним 0,28 нм.
33. Середня довжина вільного пробігу l1 молекул водню при нормальних умовах становить 0,1 мкм. Визначте середню довжину їх вільного пробігу при тиску 0,1 мПа, якщо температура газу залишається незмінною.

34. При температурі 300К і деякому тиску середня довжина вільного пробігу l молекул кисню дорівнює 0,1 мкм. Чому дорівнює середнє число зіткнень, які долають молекулами за 1 с, якщо посудина відкачати до 0,1 початкового тиску? Температуру газу вважати постійною.

35. Визначте: 1) щільність p повітря в посудині; 2) концентрацію n його молекул; 3) середню довжину вільного пробігу (l) молекул, якщо посудина відкачано до тиску 0,13 Па. Діаметр молекул повітря прийміть рівним 0,27 нм. Температура повітря 300 К.

36. Визначте коефіцієнт теплопровідності λ азоту, що знаходиться в деякому обсязі при температурі 280 К. Ефективний діаметр молекул азоту дорівнює 0,38 нм.

37. Кисень знаходиться при нормальних умовах. Визначте коефіцієнт теплопровідності λ кисню, якщо ефективний діаметр його молекул дорівнює 0,36 нм.
38. Простір між двома паралельними пластинами площею 150 см 2 кожна, що знаходяться на відстані 5 мм одна від одної, заповнене киснем. Одна пластина підтримується при температурі 17 С, інша - при 27 С. Визначте кількість теплоти, що минув за 5 хв за допомогою теплопровідності від однієї пластини до іншої. Кисень знаходиться при нормальних умовах. Ефективний діаметр молекул кисню вважати рівним 0,36 нм.

39. Визначте коефіцієнт дифузії D кисню при нормальних умовах. Ефективний діаметр молекул кисню прийміть рівним 0,36 нм.

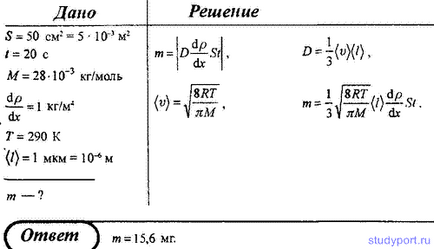
40. Визначте масу азоту, що пройшов у слідстві дифузії через площадку 50 см 2 за 20 с, якщо градієнт щільності в напрямі, перпендикулярному майданчику, дорівнює 1 кг / м 4. Температура дорівнює 290 К, а середня довжина вільного пробігу молекул дорівнює 1 мкм.
41. Визначте, у скільки разів відрізняються коефіцієнти динамічної в'язкості η вуглекислого газу і азоту, якщо обидва газу знаходяться при однакових температурі і тиску. Ефективні діаметри молекул цих газів рівні.

42. Визначте коефіцієнт теплопровідності азоту, якщо коефіцієнт динамічної в'язкості для нього при тих же умовах дорівнює 10 мкПа * c.

43. Азот знаходиться під тиском 100 кПа при температурі 290 К. Визначте коефіцієнти дифузії D і внутрішнього тертя η. Ефективний діаметр молекул азоту прийняти рівним 0,38 нм.
44. Нижче якого тиску можна говорити про вакуум між стінками судини Дьюара, якщо відстань між стінками посудини є рівним 8 мм, температура 17 С, ефективний діаметр молекул повітря дорівнює 0,27 нм.

45. Тиск розрідженого газу в рентгенівській трубці при температурі 17 ° С дорівнює 130 мкПа. Чи можна вести розмову про високому вакуумі, якщо характерний розмір l0 (відстань між катодом і анодом трубки) становить 50 мм? Ефективний діаметр молекул повітря прийміть рівним 0,27 нм.
