Мідно цинковий акумулятор саморобний своїми руками
Чи не чули про такий акумулятор.
І я не чув. Але зате матеріали для виготовлення доступні, і кожен може зібрати такий, щоб зрозуміти як працюють акумулятори.
Тому розповідаю як все вийшло і як це працює.
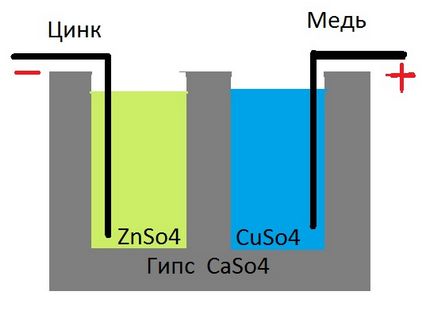
Беремо гіпс (алібастр) і відливаємо з нього таку ємність. як показано на малюнку.
Заливаємо в одну ємність Мідний купорос, а в іншу ZnSo4
На плюс в CuSo4 ставимо мідну пластину,
а на мінус в розчин ZnSo4 ставимо цинк.
Вау. у нас вийшов гальванічний елемент.
потенціал цинкового електрода - 0,76 В,
а мідного +0,34 В.
Напруга отриманого елемента дорівнюватиме 0,34 + 0,76 = 1,1 В
Давайте розглянемо - Що там відбувається. чому йде струм і що там змінюється.
Все це можливо завдяки "чудо" -мембране з гіпсу.
З'єднання CuSo4 і ZnSo4 настільки "товсті". що не можуть пролізти через решітку з гіпсу.
Гіпс у нас складається з CaSo4, тому він не реагує ні з тим. ні з цим розчином.
Напевно всі знають, якщо налити в посудину з гіпсу воду, то вода не буде з нього виливатися, але стінки судини при цьому будуть мокрі.
Через таку решітку можуть пролізти тільки іони і частково вода.
Коли ми починаємо споживати з нього струм -
Цинк на мінусі починає приєднувати до себе іони So4. які відриваються від CuSo4 в сусідній комірці і біжать через гіпсову грати.
А мідь починає наростати на плюсовій пластині.
В результаті при тривалій роботі Цинк весь перейде в розчин. а на плюсовій платівці виростить шар міді.
Тепер включаємо підзарядку цього акумулятора.
Подаємо плюс на мідь.
вона починає переходити назад в розчин (приєднує йони So4)
забирає їх у ZnSo4
при цьому йде нарощування цинкової пластини.
Акумулятор знову заряджений і готовий до використання.
Це тільки наочний посібник для розуміння процесів, які відбуваються в акумуляторі.
Не варто відразу бігти і робити такий великий акумулятор з бочки,
так як даний акумулятор має низку недоліків:
Видає всього 1 вольт, замерзає при мінусовій температурі, що не компактний, якщо довго його заряджати - то вся мідь на плюсі розчиниться до кінця.