Хто придумав батарейка - коли винайшли
Строго кажучи, повсякденна назва «батарейка» є не зовсім коректним. Воно об'єднує відразу кілька видів джерел електрики, призначених для автономного живлення пристрою. Це може бути одиночний гальванічний елемент, акумулятор або з'єднання декількох таких елементів в батарею для збільшення знімається напруги. Саме це з'єднання і породило звичне для нашого вуха назву.
Батарейки та гальванічні елементи, і акумулятори є хімічне джерело електричного струму. Перший такий джерело був винайдений як це часто буває в науці випадково італійським лікарем і фізіологом Луїджі Гальвані в кінці XVIII в.
Хоча електрику як явище знайоме людству з найдавніших часів, багато століть ці спостереження не мали ніякого практичного застосування. Лише в 1600 р англійський фізик Вільям Гілберт випустив у світ наукова праця «Про магніті, магнітних тілах і про великий магніті Землі», де були узагальнені відомі на той момент дані про електрику і магнетизм, а в 1650 р Отто фон Геріке створив електростатичну машину, що являла собою сірчаний куля, насаджений на металевий стрижень. Через століття голландцеві Пітеру ван Мушенбрук вперше вдалося накопичити за допомогою «лейденської банки» першого конденсатора невелика кількість електрики. Однак воно було занадто мало для проведення серйозних експериментів. Дослідженнями «природного» електрики займалися такі вчені, як Бенджамін Франклін, Георг Рихман, Джон Уолш. Саме праця останнього про електричні схилах зацікавив Гальвані.
Справжню мету знаменитого експерименту Гальвані, що здійснив революцію в фізіології і назавжди вписав своє ім'я в науку, тепер уже ніхто і не згадає. Гальвані препарував жабу і помістив її на стіл, де стояла електростатична машина. Його помічник випадково доторкнувся вістрям скальпеля до відкритого стегнового нерва жаби і мертва м'яз несподівано скоротилася. Інший помічник зауважив, що таке відбувається тільки тоді, коли з машини витягується іскра.
Натхненний відкриттям, Гальвані почав методично досліджувати виявлене явище здатність мертвого препарату демонструвати життєві скорочення під впливом електрики. Провівши цілу серію дослідів, Гальвані отримав особливо цікавий результат, використавши мідні гачки і срібну пластинку. Якщо гачок, який тримав лапку, торкався до платівці, лапка, доторкнувшись до пластинки, негайно скорочувалася і піднімалася. Втративши контакт з платівкою, м'язи лапки негайно розслаблялися, вона знову опускалася на платівку, знову скорочувалася і піднімалася.

Луїджі Гальвані. Журнальна ілюстрація. Франція. 1880 р
Так в результаті серії кропітких дослідів і був відкритий новий джерело електрики. Сам Гальвані, втім, не думав про те, що причина відкритого ним явища контакт різнорідних металів. На його думку, джерелом струму служила сама м'яз, яка порушувалась дією мозку, що передаються по нервах. Відкриття Гальвані викликало сенсацію і спричинило за собою безліч експериментів в різних галузях науки. Серед послідовників італійського фізіолога виявився його співвітчизник фізик Алессандро Вольта.
У 1800 р Вольта не тільки дав правильне пояснення відкритого Гальвані явища, але і сконструював пристрій, що стало першим в світі штучним хімічним джерелом електричного струму, прабатьком всіх сучасних батарейок. Воно складалося з двох електродів анода, що містить окислювач, і катода, що містить відновник, що контактують з електролітом (розчином солі, кислоти або лугу). Різниця потенціалів, що виникала між електродами, відповідала в цьому випадку вільної енергії окислювально-відновної реакції (електролізу), в ході якої катіони електроліту (позитивно заряджені іони) відновлюються, а аніони (негативно заряджені іони) окислюються на відповідних електродах. Реакція може початися тільки в тому випадку, якщо електроди з'єднані зовнішньої ланцюгом (Вольта з'єднував їх звичайної дротом), по якій вільні електрони переходять від катода до анода, створюючи таким чином розрядний струм. І хоча сучасні батарейки мають мало спільного з пристроєм Вольти, принцип їх роботи залишається незмінним: це два електроди, занурені в розчин електроліту і з'єднані зовнішньої ланцюгом.
Винахід Вольти дало значний поштовх дослідженням, пов'язаним з електрикою. У тому ж році вчені Вільям Ніколсон і Ентоні Карлайл за допомогою електролізу розклали воду на водень і кисень, трохи пізніше Хемфрі Деві таким же чином відкрив металевий калій.
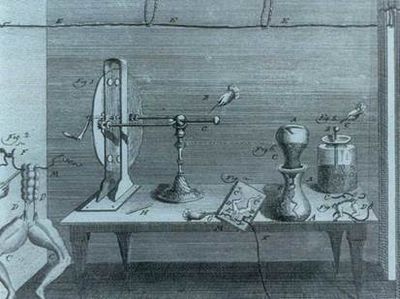
Експерименти Гальвані з жабою. Гравюра 1793 р
Але в першу чергу гальванічні елементи це, безсумнівно, найважливіше джерело електричного струму. З середини XIX в. коли з'явилися перші електроприлади, почався масовий випуск хімічних елементів живлення.
Всі ці елементи можна розділити на два основних типи: первинні, в яких хімічна реакція є незворотною, і вторинні, які можна перезарядити.
Те, що ми звикли називати батарейкою, є первинним хімічним джерелом струму, іншими словами неперезаряжаемие елементом. Першими батарейками, запущеними в масове виробництво, стали винайдені в 1865 р французом Жоржем Лекланше марганцево-цинкові елементи живлення з сольовим, а потім з загущених електролітом. Аж до початку 1940-х років це був практично єдиний вид використовуваних гальванічних елементів, який внаслідок невисокої вартості широко поширений до сих пір. Такі батарейки називають сухими або вугільно-цинковими елементами.

Гігантська електрична батарея, сконструйована У. Уолластон для експериментів X. Деві.
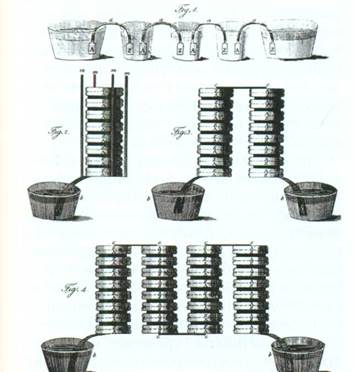
Схема роботи штучного хімічного джерела струму А. Вольти.
У 1803 р Василь Петров створив найпотужніший у світі вольтів стовп, використавши 4200 металевих кіл. Йому вдалося розвинути напругу 2500 вольт, а також відкрити таке важливе явище, як електрична дуга, яка пізніше стало використовуватися в електрозварювання, а також для електричних запалів вибухівки.
Але справжнім технологічним проривом стала поява лужних батарейок. Хоча за хімічним складом вони не особливо відрізняються від елементів Лекланше, а їх номінальну напругу в порівнянні з сухими елементами збільшено незначно, за рахунок принципової зміни конструкції лужні елементи можуть прослужити в чотири-п'ять разів довше сухих, правда, при дотриманні певних умов.
Найважливішим завданням при розробці батарей є збільшення питомої ємності елемента при зменшенні його розміру і ваги. Для цього постійно ведеться пошук нових хімічних систем. Найбільш високотехнологічними первинними елементами на сьогоднішній день є літієві. Їх ємність в два рази вище ємності сухих елементів, а термін служби значно довше. Крім того, якщо сухі і лужні батарейки розряджаються поступово, літієві тримають напругу протягом практично всього терміну служби і лише потім різко втрачають його. Але навіть найкраща батарейка не може зрівнятися за ефективністю з акумулятором, принцип дії якого заснований на оборотності хімічної реакції.
Про можливість створення такого пристрою почали замислюватися ще в XIX в. У 1859 р француз Гастон Планте винайшов свинцево-кислотний акумулятор. Електричний струм в ньому виникає в результаті реакцій свинцю і діоксиду свинцю в кислотною середовищі. Під час генерації струму розряджається акумулятор витрачає сірчану кислоту, утворюючи сульфат свинцю і воду. Щоб зарядити його, необхідно струм, що отримується з іншого джерела, пропустити по ланцюгу в зворотну сторону, при цьому вода буде використана для утворення сірчаної кислоти з вивільненням свинцю і діоксиду свинцю.
Незважаючи на те що принцип дії такого акумулятора був описаний досить давно, його масове виробництво почалося тільки в XX ст. оскільки для перезарядки пристрої потрібно струм високої напруги, а також дотримання цілого ряду інших умов. З розвитком електромереж свинцево-кислотні акумулятори стали незамінні і використовуються досі в автомобілях, тролейбусах, трамваях і інших засобах електротранспорту, а також для аварійного електропостачання.
Чимало невеликих побутових електроприладів також працюють на «багаторазових батарейках» перезаряджаються акумуляторах, що мають ту ж форму, що і невідновлювані гальванічні елементи. Розвиток електроніки безпосередньо залежить від досягнень в цій області.

Елемент живлення Ж. Лекланше.

Суха акумуляторна батарея.
Першими на зміну гальванічним елементам прийшли нікель-кадмієві та нікель-металгідридні акумулятори. Їх істотним недоліком був «ефект пам'яті» зниження ємності, в разі якщо зарядка проводилася при повному обсязі розрядженому акумуляторі. Крім того, вони поступово втрачали заряд навіть при відсутності навантаження. Ці проблеми в значній мірі були вирішені при розробці літій-іонних і літій-полімерних акумуляторів, які в даний час повсюдно використовуються в мобільних пристроях. Їх ємність значно вище, вони без втрат заряджаються в будь-який момент і добре утримують заряд в стані очікування.


Сучасне пристрій для зарядки перезаряджаються елементів АА.