Газообмін у легенях
Газообмін у легенях. Дифузія газів і газообмін
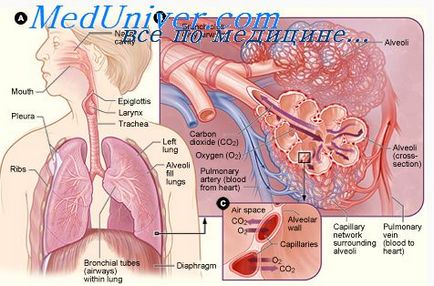
Після надходження свіжого повітря в альвеоли починається наступний етап дихального процесу: дифузія кисню з альвеол в кров і дифузія двоокису вуглецю в зворотному напрямку - з крові в альвеоли. Процес дифузії є безладний рух молекул, які прокладають собі дорогу через дихальну мембрану і рідини у всіх напрямках. Однак в фізіології дихання нас цікавлять не тільки основні механізми дифузії, але і її швидкість, що представляє собою набагато більш складну проблему і потребують більш глибоких знань в області фізики дифузії і обміну газів.
Всі гази. що представляють інтерес для фізіології дихання, є простими молекулами, які вільно переміщаються в суміші. Цей процес називають дифузією. Це справедливо і для газів, розчинених в рідинах і тканинах тіла.
Для процесу дифузії необхідна наявність джерела енергії. Енергія виробляється кінетичним рухом самих молекул. При температурі вище абсолютного нуля молекули знаходяться в постійному русі. Це означає, що вільні молекули, не пов'язані з іншими молекулами, рухаються лінійно на високій швидкості до зустрічі з іншими молекулами. Після зіткнення їх рух отримає новий напрямок - до наступного зіткнення. Таким чином, молекули перебувають у швидкому і випадковому русі серед собі подібних.
Дифузія газу одному напрямку. Вплив градієнта концентрації. Якщо в ємності або в розчині концентрація одного газу в одній зоні висока, а в іншій - низька, то сумарна дифузія газу буде спрямована від зони з високою концентрацією в зону з низькою концентрацією: на малюнку в зоні А знаходиться більше молекул, здатних рухатися в напрямку зони Б, ніж молекул, які можуть переміститися в зворотному напрямку, тому дифузія в кожному з напрямків пропорційна концентрації молекул, що на малюнку демонструє довжина стрілок.
Тиск створюється множинними ударами рухомих молекул об поверхню, тому тиск газу на поверхні дихальних ходів і альвеол пропорційно сумарної силі ударів об поверхню всіх молекул даного газу в даний момент, тобто тиск газу прямо пропорційно концентрації молекул газу.
У фізіології дихання ми маємо справу із сумішами газів, що складаються головним чином з кисню ^ азоту і двоокису вуглецю. Швидкість дифузії кожного з них прямо пропорційна тиску, який створюється тільки цим газом, і це тиск називають парціальним тиском даного газу. Далі наводимо пояснення концепції парціального тиску.
Повітря складається приблизно з 79% азоту і 21% кисню. Загальний тиск цієї суміші на рівні моря одно 760 мм рт. ст. З наведеного раніше пояснення молекулярних основ виникнення тиску ясно, що частка кожного газу в тиску їх суміші знаходиться в прямій пропорції з його концентрацією, тому 79% з 760 мм рт. ст. тиску повітря створюється азотом (600 мм рт. ст.) і 21% - киснем (160 мм рт. ст.). Таким чином, парціальний тиск азоту в суміші становить 600 мм рт. ст. парціальний тиск кисню - 160 мм рт.ст. а загальний тиск (760 мм рт. ст.) є сумою окремих парціальних тисків. Парціальний тиск окремих газів позначають Рсо2, Р02, PN2, Рн20, РНЕ і т.д.