Алкіни (ацетиленові вуглеводні) - студопедія
Для алкинов характерна тільки структурна ізомерія (ізомерія ланцюга і положення потрійного зв'язку).
З простих речовин ацетилен був отриманий вперше в XIX столітті французьким хіміком Бертло:
У промисловості ацетилен отримують крекингом метану:
Найбільш перспективним промисловим методом є отримання ацетилену з оксиду вуглецю (II) і водню в присутності каталізатора:
У лабораторії ацетилен зазвичай отримують з карбіду кальцію:
Однак, цей синтез досить дорогий, так як отримання карбіду пов'язано з високими енерговитратами:
Дешевшими методами є реакції отримання алкинов з ді-і тетра-галогенопроізводних алканів:
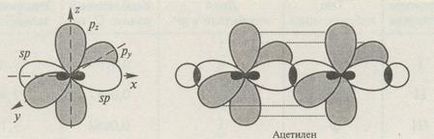
У алкінілу атоми вуглецю, які беруть участь в утворенні потрійного зв'язку, знаходяться в стані sp гібридизації:
1. Реакції приєднання (АЕ):
в) гідратація (реакція Кучерова)
д) приєднання спиртів
2. Реакції полімеризації:
а) реакція Ньюленда
б) реакція Зелінського
Горіння ацетилену в кисні супроводжується виділенням тепла, що дозволяє досягати температури до 3000 ° С (автогенная зварювання, різання металів).
На повітрі ацетилен горить коптить полум'ям, тому що в результаті неповного згоряння утворюється вуглець.
4. Освіта ацетіленід
Ацетилен і його гомологи з потрійним зв'язком на кінці молекули здатні взаємодіяти з лужними металами і солями деяких важких металів (Ag, Cu) з заміщенням водню при потрійний зв'язку на метал з утворенням ацетіленід.