Визначення заряду молекули пептиду
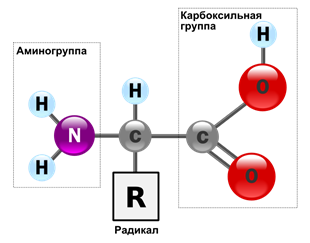
Пептиди - органічні сполуки, що складаються з амінокислот. з'єднані пептидного зв'язком.
Амінокислоти здебільшого представляють собою такі молекули:
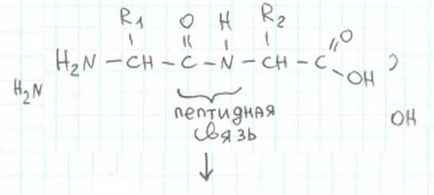
Пептидний зв'язок утворюється в такий спосіб:
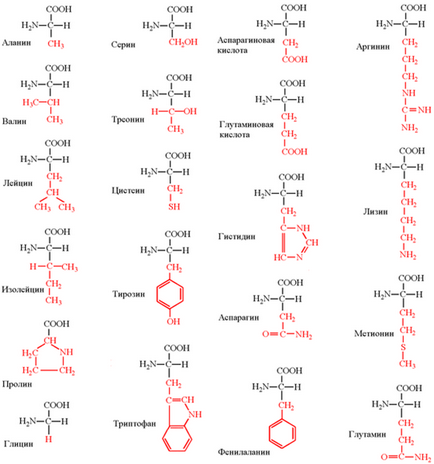
R (радикал) може бути різним. Радикали протеіногенних амінокислот, які слід вивчити, представлені в таблиці:
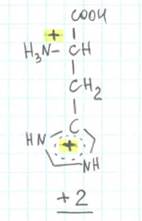
Розглянемо кілька можливих варіантів кислотності середовища:
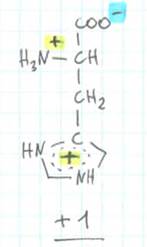
2. Менш кисле середовище близька до нейтральної, припустимо, що рН близько 5 (тобто є кількість Н + зменшується). Протонів вже не вистачає на карбоксильну групу (насамперед протон завжди втрачає саме вона), але два інших положення все ще протоновану.
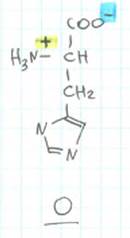
3. Нейтральне середовище і її окремий випадок - ізоелектрична точка (для гистидина це відповідає рН 7,6). У ізоелектричної точці сумарний заряд амінокислоти дорівнює нулю. Протони залишаються тільки в аминогруппе.
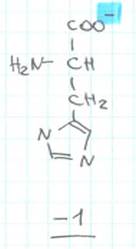
Відповідно, для того, щоб визначити заряд пептиду, необхідно визначити заряд амінокислот, що входять до його складу, в залежності від кислотності середовища.
Який заряд буде у пептиду, що складається з 3-х молекул гистидина, в дуже кислому середовищі? Для цього давайте порахуємо, скільки положень потенційно можуть протоновану (приєднати протон).
1. Дві з 3х аминогрупп і дві з 3х карбоксильних груп беруть участь в утворенні пептидного зв'язку - не можуть протоновану.
2. Вільними залишаються одна аміногрупа (N-кінець пептиду) і одна карбоксильна група (C-кінець). А також 3 імідазольних залишку.
N-кінцева аміногрупа дасть нам один плюсик, три імідазольних залишку ще 3 плюсик, а карбоксильна - нуль.
Разом. заряд пептиду His-His-His в дуже кислому середовищі дорівнює 4+
А який же заряд буде у пептиду Gly-Gly-Gly в кислому середовищі? Повторимо процедуру.
1. Дві з 3х аминогрупп і дві з 3х карбоксильних груп беруть участь в утворенні пептидного зв'язку - не можуть протоновану.
2. Вільними залишаються одна аміногрупа (N-кінець пептиду) і одна карбоксильна група (C-кінець). Радикал гліцину - Н. протоновану не може.
N-кінцева аміногрупа дасть нам один плюсик, три радикала дадуть нам три нуля, а карбоксильна ще один нуль.
Разом. заряд пептиду Gly-Gly-Gly в кислому середовищі дорівнює 1+.
Таким шляхом (розбираючи на складові) і визначається заряд пептиду.