Роль білків в організмі, природні джерела білків - студопедія
1.Роль білків в організмі, природні джерела білків.
2. Склад і будова білків.
4.Фізичні і хімічні властивості білків.
6.Превращенія білків в організмі
З органічних речовин, що входять в живу клітину, найважливішу роль відіграють білки. На їх частку припадає близько 50% маси клітини. Завдяки білкам організм придбав можливість рухатися, розмножуватися, рости, засвоювати їжу, реагувати на зовнішні впливи і т. Д.
«Життя є спосіб існування білкових тіл, істотним моментом якого є постійний обмін речовин з навколишнім їх зовнішньою природою, причому з припиненням цього обміну речовин припиняється і життя, що призводить до розкладання білка», - писав Енгельс в своїх працях.
Білки - необхідні компоненти харчових продуктів, вони входять до складу лікарських препаратів.
Білок - важливий компонент їжі людини. Основні джерела харчового білка: м'ясо, молоко, продукти переробки зерна, хліб, риба, овочі. Потреба в білку залежить від віку, статі, виду діяльності. В організмі здорової людини повинен бути баланс між кількістю вступників білків і виділяються продуктами розпаду. Для оцінки білкового обміну введено поняття білкового балансу. У зрілому віці у здорової людини існує азотне рівновагу, тобто кількість азоту, отриманого з білками їжі дорівнює кількості виділяється азоту. У молодому, зростаючому організмі йде накопичення білкової маси, тому азотний баланс буде позитивний, тобто кількість що надходить азоту перевищує кількість виведеного з організму. У людей похилого віку, а також при деяких захворюваннях спостерігається негативний азотний баланс. Тривалий негативний азотний баланс веде до загибелі організму.
Необхідно пам'ятати, що деякі амінокислоти при тепловій обробці, тривалому зберіганні продуктів можуть утворювати неусвояемие організмом сполуки, тобто ставати "недоступними". Це знижує цінність білка.
Тварини і рослинні білки засвоюються організмом неоднаково. Якщо білки молока, молочних продуктів, яєць засвоюються на 96%, м'яса і риби - на 93-95%, то білки хліба - на 62-86%, овочів - на 80%, картоплі та деяких бобових - на 70%. Однак суміш цих продуктів може бути біологічно більш повноцінним.
На ступінь засвоєння організмом білків впливає технологія отримання харчових продуктів та їх кулінарна обробка. При помірному нагріванні харчових продуктів, особливо рослинного походження, засвоюваність білків дещо зростає. При інтенсивної теплової обробки засвоюваність знижується.
Добова потреба дорослої людини в білку різного виду 1-1,5 г на 1 кг маси тіла, тобто приблизно 85-100 м Частка тваринних білків повинна складати приблизно 55% від загального його кількості в раціоні.
Багато органічних сполук, що входять до складу клітини, характеризуються великими розмірами молекул. Як називаються такі молекули? (Макромолекули) Вони складаються зазвичай з повторюваних схожих по будові низькомолекулярних з'єднань, пов'язаних між собою ковалентними зв'язками. Їх будова можна порівняти з намистинками на нитки. Як називаються ці складові елементи? (Мономери). Вони утворюють полімери. Більшість полімерів побудовано з однакових мономерів. Такі мономери називаються регулярними. Наприклад, якщо А - мономер, то -А-А-А- ...... .А- полімер. Полімери, у яких мономери різні за будовою, називаються нерегулярними. Наприклад, -А-В-Р-П-А- ...... Г-Р-П-А-. Склад визначає їх властивості.
Білки - нерегулярні полімери, мономерами яких є амінокислоти.
Білки - це складні високомолекулярні природні сполуки, побудовані з амінокислот. До складу білків входить 20 різних амінокислот, це означає величезне різноманіття білків при різних комбінаціях амінокислот. Як з 33 букв алфавіту ми можемо скласти нескінченне число слів, так з 20 амінокислот - безліч білків. В організмі людини налічується до 100000 білків.
До складу більшості білків входять 300-500 амінокислотних залишків, але є й більші білки, що складаються з 1500 і більше амінокислот. Білки розрізняються і складом амінокислот і числом амінокислотних ланок, і особливо порядком чергування їх в поліпептидних ланцюгах. Розрахунок показує, що для білка, побудованого з 20 різних амінокислот, що містить в ланцюзі 100 амінокислотних залишків, число можливих варіантів може скласти 10130. Багато білки великі і по довжині, і по молекулярній масі.
Білки повинні бути при такій масі довгими нитками. Але їх макромолекули мають формулу компактних куль (глобул) або витягнутих структур (фібрил).
Білки поділяють на протеїни (прості білки) і протеїди (складні білки). Число амінокислотних залишків, що входять в молекули, по-різному, наприклад: інсулін - 51, міоглобін - 140. Звідси Mr білка від 10 000 до кількох мільйонів.
Перша гіпотеза про будову молекули білка була запропонована в 70-х роках XIX ст. Це була уреідная теорія будови білка. У 1903 р Німецький вчений Е.Г.Фішер запропонував пептидную теорію, яка стала ключем до таємниці будови білка. Фішер припустив, що білки являють собою полімери із залишків амінокислот, з'єднаних пептидним зв'язком NH-CO. Ідея про те, що білки - це полімерні освіти, висловлювалася ще в 1888 році українським вченим А.Я.Данілевскім. Ця теорія отримала підтвердження в наступних роботах. Згідно поліпептидного теорії білки мають певну структуру
Багато білки складаються з декількох поліпептидних частинок, які складаються в єдиний агрегат. Так, молекула гемоглобіну (С738Н1166S2Fe4O208) складається з чотирьох субодиниць. Відзначимо, що Mr білка яйця = 36 000, Mr білка м'язів = 1 500 000.
Первинна структура білка - послідовність чергування амінокислотних залишків, здійснюється за рахунок пептидних (амідних) зв'язків, всі зв'язки ковалентні, міцні.
Вторинна структура - форма поліпептидного ланцюга в просторі. Білкова ланцюг закручена в спіраль, здійснюється за рахунок безлічі водневих зв'язків.
Третинна структура - реальна тривимірна конфігурація, яку приймає в просторі закручена спіраль Третинна структура - клубок з поліпептидного спіралі. (Демонстрація клубка з еластичного шнура).
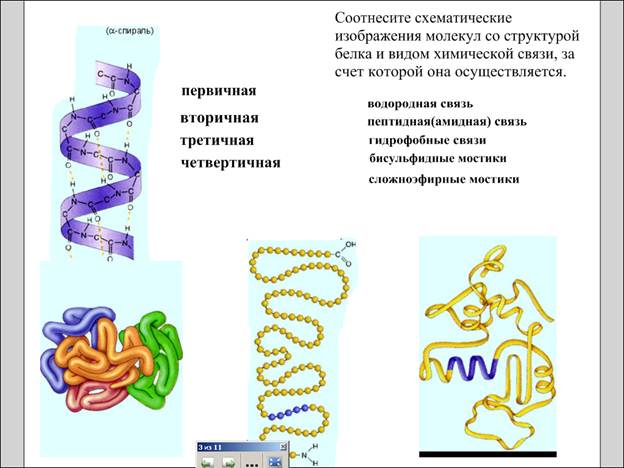
Уявити конфігурацію легко, важче зрозуміти, які сили її підтримують. (Водневі зв'язку, дисульфідні містки -SS-, складноефірний зв'язок між радикалами. Полярні групи COOH і OH взаємодіють з водою, а неполярні радикали відштовхують її, вони спрямовані всередину глобул. Радикали взаємодіють між собою завдяки силам Ван-дер-Ваальса.) (За рахунок гідрофобних зв'язків), у деяких білків - S-S-зв'язку (бісульфідні містки), складноефірні містки ..
Четвертичная структура - з'єднані один з одним макромолекули білків утворюють комплекс. Четвертичная структура - структура з декількох поліпептидних ланцюгів