Концентрація позначення - довідник хіміка 21
Мал. У1П-28. Спосіб позначення концентрацій в т-ступеневу каскаді.
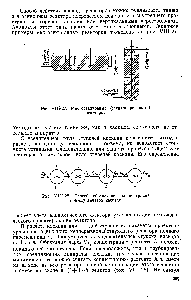
Вимірювані і регульовані параметри 1 - температура Р - тиск С - витрата С - концентрація. Позначення приладів Я-показує Сг-який сигналізує С-самопишущий І - інтегруючий Яз-ізодромний [c.691]
При перевірці насамперед обчислюють ціну поділки шкали обох ареометрів. Для цього знаходять різницю значень щільності (концентрації), позначених на двох сусідніх основних (циф-.рових) штрихах шкали. і ділять різницю на число поділок. укладених між цими штрихами. Крім того, визначають всі інші характеристики ареометрів, зазначені на шкалах, і заносять їх до протоколу повірки. [C.568]
Далі позначення ppm і% відповідають масовим концентраціям. позначення ppm об. і% об. - об'ємним. [C.6]
Якщо ввести для молярних концентрацій позначення Xq, Xq, у і j k для Ao.Aq. з і АОС відповідно, то для реакцій (А) і (В) ми можемо написати закон діючих мас у вигляді [c.65]
Тут концентрація речовини зменшується і в анодному, і в катодному просторах. Зберігаючи колишні позначення, тепер можна написати [c.108]
Верхній індекс у позначення граничних концентрацій вказує ту ОПК, по якій вони беруться. Так, в даному випадку, коли визначається мінімальна флегмовое число. при якому з дистиляту зникає -й комнонент, необхідно користуватися граничними концентраціями ОПК. яка не містить (/ - - 1) -го компонента. [C.360]
Рішення сформульованої вище задачі оптимізації зручніше провести в два етапи. Іа першому етапі можна визначити, як повинна змінюватися концентрація х. реагенту, 4 але довжині реактора для того, щоб забезпечити максимум вираження (VII, 312), яке з урахуванням позначень (VII, 315) може бути записано як [c.370]
Такий спосіб поділу реакційної зони на частини, в яких умови проведення процесу різні, називається секціонуванням апарату. На рис. 1Х-74 нанесена крива рівноважних концентрацій аміаку в залежності від температури (р = 300 ат). Гази надходять в реактор з теплообмінника при температурі 450 ° С. Реагуючи в першій секції реактора (перший шар каталізатора), гази нагріваються в результаті виділення теплоти реакції в умовах, близьких до адиабатическим реакційна суміш майже досягає стану рівноваги. позначеного точкою Л (/ 635 ° С). Після проходження через перший шар каталізатора гази знову охолоджуються до температури 450 ° С. У другій секції, де відбувається подальше перетворення, реакційна суміш наближається до стану рівноваги. що відповідає точці В на кривій. У подальших етапах проведення процесу досягаються стану, близькі до точок С, О і Є. Як випливає з рис. 1Х-74, висота шарів каталізатора в напрямку руху потоку зростає, оскільки швидкість перетворення зменшується дуже швидко. [C.424]
В якому позначення констант відповідають наведеним на стор. 85. При постійній концентрації протонів [Н "] експериментально було доведено, що записана нижче дріб теж є постійною величиною [c.87]
Склади ідеального розчину і його насиченої пари різні. т. е. УФХ. В даному випадку легко знайти зв'язок між у я X. видання насправді. концентрація другого компонента в парі у = р 1р. Підставивши в цей вираз значення р з рівняння (VI, 10а) та значення р з рівняння (Ч, 11) і ввівши позначення Рур -а, отримаємо [c.189]
У цих рівняннях, згідно з прийнятими нами позначенням, а, л і у - стаціонарні концентрації компонентів А, X і V в реакторі відповідно V - об'єм рідини в ньому і та - об'ємна швидкість потоку. Так як швидкість продукту на виході з апарату дорівнює їх, а швидкість надходження свіжого реагенту повинна дорівнювати і (а + х + у), то вихід [c.111]
Виходячи з рівнянь ліній концентрацій нижньої і верхньої секцій колони і ввівши позначення х і у для координат точкж їх перетину, можна записати [c.173]
Таких рівнянь можна написати стільки, скільки є в системі компонентів. Другий нижній індекс у позначення концентрацій в даному випадку опущений для того, щоб підкреслити, що ці рівняння перерахунку псевдоконцентрацій можуть застосовуватися для будь-якої тарілки. З виразів (V.23) і (VIII.109) безпосередньо випливає, що сума псевдоконцентрацій також дорівнює одиниці [c.413]
Маючи 1 пиду. що Рі, 2 - = Ра1- ра си. ріо. 11.1), І ввсдя позначення Рі, т для среднелогаріфміческого парціального тиску комнонента і> і позначення для сроднологаріфміческого значення його кінцевих концентрацій [c.66]
Виходячи з рівнянь кривих концентрацій верхньої і нижньої секцій колони і вводячи позначення Х і в1 для коордніат їх точки перетину. маємо [c.187]
Верхній індекс у позначення граничних концентрацій вказує ту ОПК, по якій онп беруться. Так, в даному випадку, коли визначається мінімальна парове число. при якому з залишку зникає j-ii компонепт, пеобходімо користуватися граничними концентраціями OHKj), в.о. містить (/ -1,) - го компонеіта- [c.347]
У денствптелигостп стандартний стан але може бути станом прп нескінченному ра. шеденні, так як воно має представляти собою певне термодинамічний стан з фіксованим складом. Ми розуміємо йод нескінченним розведенням такий стан системи, в якому взаємодія між частинками розчиненої речовини дуже малий, і в реальному стандартному стані система буде мати, отже, деякий склад. відповідає цьому ідеальному умові. На практиці найчастіше для позначення концентрації користуються молярна, а за стандартний стан зазвичай вибирається гіпотетичний одномолярний розчин. т. е. 1 М розчин, в якому взаємодія розчиненої речовини і розчинника дорівнює нулю. [C.431]
На рис. XVII. точкп, позначені гуртком, відносяться до изотерме Фрейндліха, яка при 0 = 0,665 і 0 = 0,86 відповідає складної изотерме Ленгмюра. В діапазоні концентрацій (Л) / Л 2,1 від 0,5 до 8 обидві ізотерми мають максимальне розбіжність па 8% і середнє розбіжність приблизно на 2%, що вказує па гарне відповідність. яке може бути досягнуто між ППМП. Підбором інших параметрів можна було б встановити відповідність і для боліе низьких тисків. [C.539]
Структурний застигання нафтових продуктів викликається утворенням в них при охолодженні твердої фази, частинки якої. досягнувши відомої концентрації, зв'язуються між собою і утворюють структуру. мобілізують всю масу продукту. Речовинами, здатними виділятися з нафт і нафтових продуктів описаним вище чином, є що містяться в них кристалізуються парафінові вуглеводні. Природа цих речовин була пояснена ще в двадцятих роках В. С. Твер-ціпим [21], Б. Г. Тичинін [22], Л. Г. Гурвич [23], Н. Д. Граменіцкий [24], Гольде [25 ] і іншими дослідниками і далі підтверджена численними подальшими роботами. Тут слід тільки уточнити, що термін парафіни потрібно розуміти в даному випадку не як позначення вуглеводнів ряду алканів. а як найменування твердих, здатних кристалізуватися вуглеводнів нафти. в число яких можуть входити, не тільки власне парафінові вуглеводні. але і тверді кристалічні нафтенові і ароматичні вуглеводні. Загальним для цих вуглеводнів є їх здатність виділятися в тих чи інших кристалічних формах з розчину в нафтових продуктах при охолодженні. [C.14]
Тоді, користуючись цими та раніше введеними позначеннями, розрахуємо концентрацію етилу [1етата в вихідної суміші [c.255]
За рівнянням (IX, 38), (1Х, 39) і (1Х, 40) знаходимо fe = 2, l см / сек k = = 0,035 см1сек а = 2,91 см (в цьому прикладі символом позначений коефіцієнт массоотдачи в газовій фазі . в якому рушійна сила виражена в одиницях концентрації. на відміну від кд, для якого вона виражається в одиницях парціального тиску). [C.201]